配制溶质质量分数一定的氯化钠溶液常有以下操作。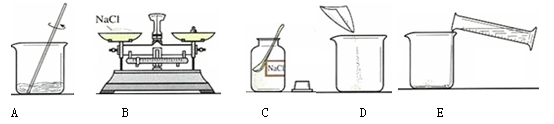
请回答下列问题:
(1)用上图所示的序号表示配制该溶液的正确操作顺序为 。
(2)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应 。
| A.增加适量氯化钠固体 | B.减少适量氯化钠固体 |
| C.调节游码 | D.添加砝码 |
(3)将氯化钠和水依次倒入烧杯中,用玻璃棒搅拌,其目的是 。
用化学符号和数字填空:
(1)2个铵根离子;(2)3个氮气分子。
化学是一门以实验为基础的科学。实验室里现有高锰酸钾、大理石和稀盐酸,以及下列仪器,回答有关问题:
(1)利用上述仪器和药品做"制取二氧化碳的实验",反应的原理是(用化学方程式表示);选择仪器后,连接装置并检查。
(2)若补充一种玻璃仪器(填仪器名称),利用上述仪器和药品还可以制取氧气,你选择的仪器是(填序号),反应的化学方程式为。
二氧化碳的"捕捉"与"封存"是实现温室气体减排的重要途径之一。实际生产中,经常利用足量
溶液来"捕捉"
,流程图如下(部分条件及物质未标出)。
(1)分离室中进行的操作是。
(2)该流程图所标出的物质中,溶于水放出大量热的氧化物是。
(3)"捕捉室"内发生反应的化学方程式为。
(4)将
加入到x溶液中,其中发生复分解反应的化学方程式是。
金属及金属材料在生产、生活中应用广泛。
(1)铜可以拉成铜丝,这是利用金属的_________。
(2)铝具有很好的抗腐蚀性能,原因是____________________(用化学方程式表示)。
(3)小明在学习金属的化学性质时,做了如下探究实验(金属片已打磨):
①将铁片插入硫酸铜溶液中,铁片表面的现象是_____________________;
②将铜片插入硝酸银溶液中,反应的化学方程式是__________________。
此探究实验的目的是________________________________。
化学与生活密切相关。
(1)米饭、馒头能提供的营养素主要是。
(2)日常生活中鉴别棉纤维与涤纶,可用的方法。
(3)天然气是家用燃料之一,其主要成分是(写化学式)。
(4)食醋的主要成分是醋酸(
)。醋酸由种元素组成,其中氢元素与氧元素的质量比为(结果用最简整数比表示)。