(11分)氧气和二氧化碳是初中化学常见的两种重要物质。请你参与下列氧气和二氧化碳有关制备、转化的实验探究活动。
Ⅰ:实验室制取氧气和二氧化碳。
(1)用高锰酸钾制取氧气,发生反应的化学方程式是 。如果要制得较纯净的氧气,应该选择装置 (填上述装置图示中序号)收集。
(2)制取二氧化碳,可选择图示中B与F组合为装置,需要的化学药品是 ;向B中加入药品前的一步实验操作是 。该组合装置既可用于制取二氧化碳又可用来制取氧气,其中选用相同发生装置制取二氧化碳和氧气的原因是 。
Ⅱ:用过氧化钠反应来制取氧气,是潜水员使用的供氧装置的原理。
【查阅资料】常温常压下过氧化钠是淡黄色固体,在不需要加热的情况下能与二氧化碳反应生成氧气和另一化合物(生活中常见的盐);过氧化钠能与水反应生成氧气和氢氧化钠。
【设计装置】为验证过氧化钠(Na2O2)和CO2反应原理,设计如下实验装置。
【实验操作】向装置X中通入足量CO2气体,观察到X瓶中的淡黄色固体逐渐变为白色粉末,同时见到Y、Z装置中有气泡出现。
【实验分析】
(3)过氧化钠与二氧化碳反应除生成氧气外,另一化合物的化学式为 ;Y中的溶液是 ;Z中浓硫酸的作用是 。
(4)验证过氧化钠和二氧化碳反应生成氧气的操作是 。
(5)反应结束后,可设计一个简单实验,验证X瓶中过氧化钠是否有剩余(除用二氧化碳验证外),其实验原理是 (用化学方程式表示)。
人体的汗液有咸味。小庭和小怡同学猜测汗液中可能含有氯化钠,为此她们准备做探究实验。她们想到两种提取汗液的方法,方法一:用胶头滴管直接吸取足量汗液转移到烧杯中,再加入适量蒸馏水稀释;方法二:用出汗的手在盛有自来水的容器中清洗,再将清洗后的自来水部分转移到烧杯中。其中方法 是正确的。
在老师指导下,她们用正确的方法提取汗液,进行以下实验:
(1)用试管取适量提取液,滴入硝酸钡溶液,没有出现白色沉淀,说明汗液中 (填:“有”或“无”)硫酸和硫酸盐。
(2)用试管取适量提取液,滴入硝酸银溶液,发现有白色沉淀出现,加入稀硝酸后沉淀不溶解。由此可推测该白色沉淀物的化学式是 。
(3)将适量提取液倒入蒸发皿中加热蒸发,出现类似食盐的小颗粒。
你认为她能否仅凭上述三步实验得出“这些小颗粒就是氯化钠”?
由于大量使用一次性塑料方便袋而造成的“白色污染”已成为一个严重的社会问题。某化学研究小组的同学对某种塑料袋的组成进行分析研究(资料显示该塑料只含C、H两种元素)。他们设计了图18所示的实验装置,使该塑料试样在纯氧中完全燃烧,观察实验现象、分析有关数据、推算元素含量。
(1)实验装置中有一处明显错误,请指出错误处,并写出(或在答题卷上画出正确图并用字母标注上哪一个装置)改正方法
(2) 装置F的作用是.
(3) 若装置C的玻璃管中放入的塑料试样质量为5.9g,塑料试样充分燃烧后,装置D增重7.2g,则该塑料试样中含氢元素的质量为g;假设塑料的组成为CxHy,则装置C的玻璃管中反应的化学方程式为(化学计量数用含x、y的代数式表示,且可以是分数)
(4)若装置中没有连接装置B,将使该塑料试样中氢元素的质量测算结果( 填“偏小”、“ 偏大”或“无影响” )
.绿色植物的呼吸作用会产生二氧化碳,小明猜想:种子的萌发过程可能也会产生二氧化碳,他设计了如图实验装置。打开D装置中的阀门,水位下降,空气就会依次进入装置。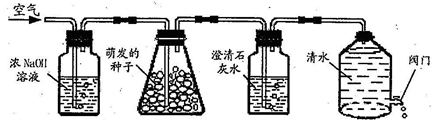
ABC D
(1)按照实验设计意图,如果观察到C装置中澄清石灰水变浑浊现象,则小明的猜想是正确的。但思维严密的小庭却认为实验还有漏洞,她建议在(选填:AB、BC或CD)之间再增加一个C装置,就可以弥补上图实验设计的不足,那么,改进后的实验装置中,当观察到现象时才能证明小明的猜想是正确的。
(2)请指出D装置的一个优点:。
请参与某学习小组进行研究性学习的过程,并协助完成相关任务:
[提出问题] 在平时探讨酸的性质时,我们通常是讨论酸的水溶液。究竟水在酸显示酸的特性时扮演什么角色呢?
[确定研究对象] 以我们最熟知的盐酸(氯化氢的水溶液)和氯化氢进行探究。[查阅资料] 氯化氢溶于水时解离出氢离子和氯离子,而溶于干燥的甲苯(一种有机溶剂)时仍以氯化氢分子的形式分散(如下图)。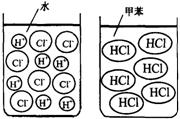
[设计与实验] (请完成下表)
| 实验内容 |
实验现象 |
解释与结论 |
| 测定导电性 |
氯化氢的水溶液:导电性良好 |
氯化氢的水溶液中有自由移动的离子 |
| 氯化氢的的甲苯溶液:A |
氯化氢的甲苯溶液中没有自由移动的离子 |
|
| 与镁作用 |
氯化氢的水溶液: B |
化学方程式: C |
| 氯化氢的甲苯溶液:没有明显的现象 |
氯化氢在甲苯溶液中没有解离出氢离子 |
|
| 与固体碳酸钠的作用 |
氯化氢的水溶液:产生气泡 |
化学方程式: D |
| 氯化氢的甲苯溶液: |
氯化氢在甲苯中没有解离出氢离子 |
[讨论与反思] 盐酸的酸性是因为氯化氢在水分子的作用下解离出了_______________E____。
小黎同学为了进一步加深对“碱的化学性质”的理解,特邀你协助完成下列活动与探究:
(1) 如右图所示,在白色点滴板上进行实验,请将实验现象填入下表:
| 氢氧化钠溶液 |
氢氧化钙溶液 |
|
| 加紫色石蕊溶液 |
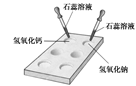
(2)回忆检验二氧化碳气体的反应,写出该反应的化学方程式。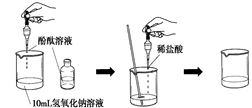
(3)三氧化硫(SO3)与氢氧化钠反应与上面的反应类似,写出这一反应的化学方程式。
(4)如右图所示,在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞试液,溶液显色,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成
为止。
这一实验说明:酸与碱作用生成了盐和水,这一反应叫做反应。中和反应的实质是;实验中滴加酚酞的作用是。
(5)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙有哪些相似的化学性质。(任写两点)
①②