(1)下图为实验室制备、收集少量HCl的装置。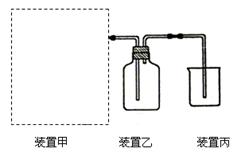
①制备HCl所用药品为浓硫酸和浓盐酸,则甲的最佳装置应选用下图中的 。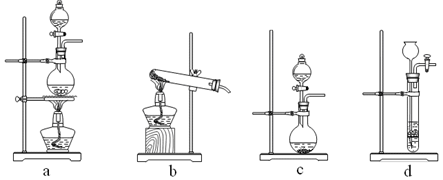
② 请解释能用浓硫酸和浓盐酸制备HCl气体的原因 。
③ 装置丙用来吸收过量的HCl气体,为防止倒吸,则烧杯中应该装入水和 。
(2)以下为苯的取代反应的探究实验。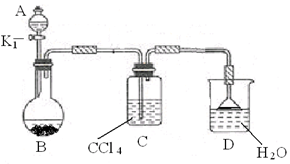
① 按上图所示的装置图连接好各仪器。
② 检验装置的气密性。
③ 在A中加入适量的苯和液溴的混合液体,在B中加入少量铁粉,塞上橡皮塞,打开K1,开始进行反应,放入适量混合液后,关闭K1。
写出B中发生反应的化学方程式 。
装置C的作用是 。
④ 反应结束后,用试管取少量D中的溶液,加入
(描述试剂和现象),则证明B中的取代反应已经发生。
⑤ 把B中的固液混合物体过滤,分离出液体混合物,按下图方案精制含有苯和溴的溴苯。
其中试剂为 ,操作名称为 。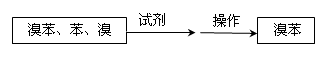
利用化合价推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
①SO2的性质________________(填序号,下同)
A.只有氧化性B.只有还原性C.既有还原性又有氧化性
②SO2通入酸性KMnO4溶液中,溶液由紫色褪至无色。反应后,锰元素被还原成Mn2+,写出上述反应的离子方程式_________________________________
(2)Fe(OH)2很不稳定,露置在空气中容易被氧化,发生反应的离子方程式为__________________________________________________为了获得白色的Fe(OH)2沉淀,可以用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配置的NaOH溶液反应制备。
①用硫酸亚铁晶体配置上述硫酸亚铁溶液时,还需加入_________来防止Fe2+被氧化
②除去蒸馏水中溶解的O2常采用_______的方法
(3)检验Fe3+的方法:_______________________(写出加入试剂的化学式和现象与结论)
按要求写下列化学方程式(1)、(4)或离子方程式(2)(3)
(1)实验室用Ca(OH)2和NH4Cl制取氨气_______________________________
(2)过氧化钠粉末投入水中_____________________________________________
(3)向氯化铝溶液中加入足量氨水_______________________________________
(4)漂白粉在空气中变质_______________________________________________
实验室有化学纯的浓硫酸,其试剂瓶标签上的部分内容如下图:
请回答下列问题:
(1)实验室只有100 mL、250 mL、500 mL三种规格的容量瓶,但要配制480 mL 0.50 mol/L的稀硫酸,需取该浓硫酸mL。
(2)接下来完成此实验你将用到的仪器有20 mL量筒、烧杯、玻璃棒、____________。
(3)要从所配溶液中取出50 mL盛装于试剂瓶中,给它贴上标签,则标签的内容是________________;若再从中取出10 mL溶液稀释至20 mL,则稀释后溶液的物质的量浓度为__________。
(4)下列操作会使所配溶液浓度偏低的是。
| A.用量筒量取浓硫酸,读数时仰视刻度线 |
| B.转移溶液时未洗涤烧杯 |
| C.容量瓶用蒸馏水洗净后仍残留有蒸馏水 |
| D.定容时俯视容量瓶的刻度线 |
E.定容摇匀后,发现液面低于刻度线,再加水至刻度线
A、B、C、D表示中学化学中的四种常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去)。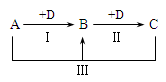
(1)若A为强碱溶液,其焰色反应显黄色,C为厨房中用品,请回答下列问题:
①D的化学式是。
②反应III的离子方程式是。
③现有B和C的固体混合物a g,加热至质量不再改变时剩余固体 b g,则B的质量分数为_______________。
(2)若A、D均为单质,且A为黄绿色气体,D的一种红棕色氧化物常用作颜料,则:
①反应III的离子方程式是。
②取少许C溶液于试管中,滴入NaOH溶液并振荡,发生反应的化学方程式为:______________________________,________________________________。
③检验C溶液中金属阳离子的操作是。
镁与稀硝酸的反应为:Mg+ HNO3(稀)—— Mg(NO3)2+ NH4NO3+ H2O
(1)配平上述化学方程式并用“双线桥法”表示该反应中电子转移的方向和数目。
(2)该反应中,还原产物是_________,HNO3表现了________(选填“还原性”、“氧化性”、“酸性”、“碱性”)。
(3)若反应过程中转移的电子数为6.02×1023,则被还原的硝酸物质的量为________。