(10分)为了测定某样品中氧化铁(Fe2O3)的质量分数(杂质不含铁元素,且不溶于水和酸),某兴趣小组的同学进行了如下的实验,请你参与过程分析。
【查阅资料】
1.草酸(H2C2O4)在浓硫酸作用下受热分解,化学方程式为H2C2O4  CO2↑+CO↑+H2O
CO2↑+CO↑+H2O
2.碱石灰能吸收二氧化碳和水蒸气
【实验设计及操作】用下图所示装置进行实验: 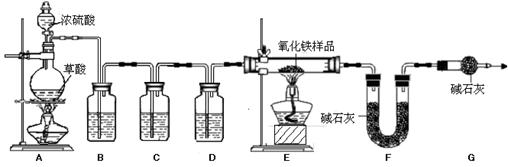
【问题讨论】
⑴装药品前应先 ,实验中观察到E中现象是:固体颜色 ;
⑵进入E中的气体是纯净、干燥的CO,则B、C、D中依次是 (填序号)。
① 浓硫酸、石灰水、氢氧化钠溶液 ② 石灰水、氢氧化钠溶液、浓硫酸
③ 氢氧化钠溶液、石灰水、浓硫酸
⑶ G的作用是 ;E中反应的化学方程式是 ;
⑷当E中固体完全反应后,先熄灭 灯(A、E);
⑸实验装置有一明显缺陷是: 。
【数据处理】称取样品8.0g,用上述装置进行实验,充分反应后称量F装置增重4.4g。则样品中氧化铁质量分数为 。
【实验反思】当观察到E中固体全部变黑后,若立即停止通CO,则测得的样品中氧化铁的质量分数 (填“偏大”,“偏小”,“无影响”)。
金属材料被广泛地应用于我们的生活中,不仅是因为其物理性能优良,还与它们的化学性质密切相关。下面是小明同学设计测定金属铁、铜和镁的活动性的探究实验过程和实验记录,请你一起探究。
【实验记录】测定金属铁、铜和镁的活动性强弱
【所用试剂】稀硫酸、硝酸银溶液、光亮的薄铁片、薄铜片、薄镁片
【实验过程】
步骤Ⅰ将铁片、铜片、镁片分别在空气中点燃片刻,观察燃烧现象;
步骤Ⅱ将铁片、铜片、镁片分别放入三支盛有浓度相同、体积相同的稀硫酸的试管中;
步骤Ⅲ将铁片、铜片、镁片分别放入三支盛有浓度相同、体积相同的硝酸银溶液的试管中。
【实验记录】用“√”表示能观察到实验现象,用“-”表示观察不到实验现象(见下表)。实验现象记录如下表
| 金属 |
空气 |
稀硫酸 |
硝酸银溶液 |
| 铁 |
- |
√ |
√ |
| 铜 |
- |
- |
√ |
| 镁 |
√ |
√ |
√ |
(1)通过步骤Ⅰ可以得出三种金属中镁的金属活动性最强,判断依据是_______。
(2)运用“控制变量法”设计实验方案是化学研究的重要方法。步骤Ⅱ和步骤Ⅲ中,需要控制的实验条件除了金属的体积、溶液的体积、溶液浓度以外,还需要控制的条件是_______________________,写出镁和稀硫酸反应的化学方程式_______________,此反应属于________________________。
【实验结论】金属铁、铜和镁的活动性由强到弱的顺序是__________(用元素符号表示)。
【反思交流】若利用上述试剂制取氢气,小明认为应该选择金属铁和稀硫酸反应,而不选择金属镁和稀硫酸反应,他的理由是______________。
下图是探究铁制品锈蚀的条件时做的五个实验(铁钉在不同环境中),实验一段时间后,得出的结论错误的是( )
| A.甲、乙、戊中铁钉生锈快慢的顺序为乙>甲>戊 |
| B.丙中的铁钉不生锈 |
| C.铁生锈的主要条件是与空气、水直接接触 |
| D.丁中铁钉生锈最严重 |
小芳同学从超市购买了一瓶维生素C泡腾片。下图是标签上的部分内容。
| 维生素C泡腾片 功能:补充人体维生素C,增强机体抵抗力 主要成分:维生素C 辅料成分:碳酸氢钠、氯化钠、酒石酸晶体、蔗糖、糖精钠、阿朴胡萝卜醛、橘味香精、橙味香精、维生素B 贮藏:低温、避光、防潮 |
小芳同学根据使用说明将维生素C泡腾片放入一杯水中,发现维生素C泡腾片逐渐溶解,产生大量气泡,片刻后变为一杯鲜甜的橙味饮品。小芳同学感到很好奇,产生的气泡是什么呢?
请你参与小芳同学的探究:
【提出问题】维生素C泡腾片放入水中,产生的气泡是什么呢?
【我的猜想】气体成分是________,理由是_________________________。
【实验方案】
| 实验步骤 |
实验现象 |
实验结论 |
| 将一片维生素C泡腾片放入水中,将产生的气体通入__ __________________ |
根据维生素C泡腾片储存条件,请说明保存时要低温和防潮的原因是:
①______________________________________________________;
②______________________________________________________。
日常生活中使用的塑料袋有两种,一种是用聚乙烯制成的,另一种是用聚氯乙烯制成的。通过查阅资料知:聚乙烯完全燃烧生成CO2和H2O,而聚氯乙烯完全燃烧除生成CO2和H2O外,还有刺激性气味的气体产生,该气体极易溶于水生成盐酸,则该气体是________________。
(1)鉴别这两种塑料袋最简单的方法是________________________________。
(2)现用如图所示的实验来探究塑料燃烧的产物。实验时,若B、C两瓶都观察到明显现象,则B瓶中的现象是_____________,C瓶中的现象是___________,由此可判断A瓶中燃烧的是_____________________。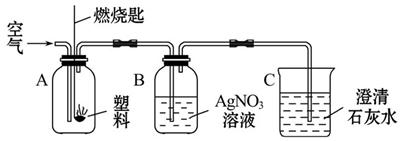
学习氢氧化钠的性质之后,知道氢氧化钠溶液中含有H2O、Na+、OH-,能使无色酚酞溶液变红色,某科技小组想进一步探究是哪一种粒子使无色酚酞溶液变红色。
【提出猜想】猜想①:可能是H2O;
猜想②:可能是Na+;
猜想③:可能是OH-。
【实验验证】
| 实验操作 |
实验现象 |
结论 |
| ①用试管取少量蒸馏水,滴入1滴~2滴无色酚酞溶液,振荡 |
试管内溶液仍为无色 |
水分子不能使无色酚酞溶液变红色 |
| ②用试管取少量氯化钠溶液,滴入1滴~2滴无色酚酞溶液,振荡 |
||
| ③用试管取少量氢氧化钠溶液,滴入1滴~2滴无色酚酞溶液,振荡 |
【讨论反思】有同学认为猜想①不需要实验验证就可以排除,你认为该同学的理由是__________________________。