铁及其化合物与生产、生活关系密切。
(1)下图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。

①该电化腐蚀称为。
②图中四个区域,生成铁锈最多的是(填字母)。
(2)用废铁皮制取铁红()的部分流程示意图如下:

①步骤I若温度过高,将导致硝酸分解。硝酸分解的化学方程式为。
②步骤Ⅱ中发生反应:,反应产生的又将废铁皮中的铁转化为,该反应的化学方程式为。
③上述生产流程中,能体现"绿色化学"思想的是(任写一项)。
(3)已知t℃时,反应的平衡常数=0.25。
①t℃时,反应达到平衡时=。
②若在1 密闭容器中加入0.02 ,并通入,t℃时反应达到平衡。此时转化率为50%,则=。
氢气、甲烷(CH4)、水各1g,其中含分子数最多的是;含氢原子最多的是;氢气、甲烷、水各1mol,含分子数是否一样多?;含氢原子数最多的是。
阅读、分析下列两个材料:
材料一、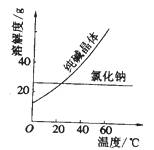
材料二、
| 物质 |
熔点/℃ |
沸点/℃ |
密度/g·cm-3 |
溶解性 |
| 乙二醇( C2H6O2) |
-11.5 |
198 |
1.11 |
易溶于水和乙醇 |
| 丙三醇(C3H8O3) |
17.9 |
290 |
1.26 |
能跟水、酒精以任意比互溶 |
回答下列问题(填写序号):
| A.蒸馏法 | B.萃取法 | C.“溶解、结晶、过滤”的方法 | D.分液法 |
(1)将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用__________。
(2)将乙二醇和丙三醇相互分离的最佳方法是__________。
填写下表:
| 粒子符号 |
质子数Z |
中子数N |
核外电子数 |
质量数A |
| Cl |
17 |
20 |
||
| S2- |
18 |
32 |
||
| Al3+ |
14 |
27 |
||
| AYm- |
y |
A |
||
| AXn+ |
x |
A |
摩尔这个单位是以________Kg12C中所含的原子数目为标准,来衡量其它粒子集体中所含粒子数目的多少。该数目的数值是个常数,被称为____________________。
现有X、Y、Z三种元素,已知有如下情况:
①X、Y、Z的单质在常温下均为气体。
② X的单质在Z的单质中燃烧,生成XZ,燃烧时火焰呈苍白色。
③ XZ极易溶于水,在水溶液中电离出X+和Z-。XZ的水溶液可使石蕊试液变红。
④两分子X的单质可与一分子Y的单质化合生成两分子X2Y,X2Y常温下为液体。
⑤ Z的单质溶于X2Y中,所得溶液具有漂白作用。
请完成下列问题:
(1)写出XZ和X2Y的化学式:XZ X2Y
(2)Z的单质溶于X2Y后,溶液起漂白作用的物质是 (写化学式)。
(3)写出X的单质在Z的单质中燃烧的化学方程式 。
(4)Z的单质能否与氢氧化钠溶液发生反应: (填“能”或“否”),若能,请写出反应的化学方程式: 。
(若不能反应,则此空不必填写)。