工业上常利用含硫废水生产,实验室可用如下装置(略去部分加持仪器)模拟生成过程。

烧瓶中发生反应如下:
(I)
(II)
(III)
(1)仪器组装完成后,关闭两端活塞,向装置中的长颈漏斗内注入液体至形成一段液注,若,则整个装置气密性良好。装置的作用是。装置中为溶液。
(2)为提高产品纯度,应使烧瓶中和恰好完全反应,则烧瓶中和物质的量之比为。
(3)装置B的作用之一是观察的生成速率,其中的液体最好选择。
a.蒸馏水 b.饱和溶液
c.饱和溶液 d.饱和溶液
实验中,为使缓慢进入烧瓶,采用的操作是。已知反应(III)相对较慢,则烧瓶中反应达到终点的现象是。反应后期可用酒精灯适当加热烧瓶,实验室用酒精灯加热时必须使用石棉网的仪器含有 。
a.烧杯 b.蒸发皿 c.试管 d.锥形瓶
(4)反应终止后,烧瓶中的溶液经蒸发浓缩即可析出,其中可能含有、等杂质。利用所给试剂设计实验,检测产品中是否存在,简要说明实验操作,现象和结论:。
已知遇酸易分解:↓↑
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、溶液、溶液
若用12 mol•L-1的浓盐酸配制0.10 mol•L-1的稀盐酸500 mL,回答下列问题:
(1)量取浓盐酸的体积为mL,如果实验室有5mL、10mL、50mL量筒,应选用mL量筒最好。若量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将(偏高、偏低、无影响)。
(2)配制时应选用的容量瓶规格为mL ,除容量瓶还需选用的仪器主要有、、和。
(3)配制时,将量取的浓盐酸沿烧杯内壁慢慢注入约100mL水里,并不断搅拌,目的是。
(4)将冷却后的上述溶液沿注入中,并用约50mL蒸馏水洗涤烧杯2~3次,转移摇匀。(填仪器)
(5)加水至距刻度线 处,改用(填仪器)滴加水,使溶液的凹液面正好跟刻度线相切,最后盖上瓶塞,摇匀。
处,改用(填仪器)滴加水,使溶液的凹液面正好跟刻度线相切,最后盖上瓶塞,摇匀。
(6)若实验遇下列情况,溶液的浓度是偏高 ,偏低还是不变?
,偏低还是不变?
| A.加水时越过刻度线______ | B.忘记将洗涤液加入容量瓶______ |
C.容量瓶内壁附有水珠而未干燥处理 |
D.溶解后没有冷却便进行定容 |
某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,控制水浴温度在85oC左右,缓慢加热至反应完全,在试管
 C内得到环己烯粗品。
C内得到环己烯粗品。
①上面的制备装置中,还缺少的玻璃仪器是,导管B除 了导气外还具有的作用是。
了导气外还具有的作用是。
②试管C置于冰水浴中的目的是
 。
。
(2)制备精品(用下图)
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在层(填上或下),分液后用(填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4c.Na2CO3溶液
②再将环己烯按下图装置蒸馏,冷却水从口(填上或下)进入。蒸馏时要加入生石灰,目的是。
③收集产品时,控制的温度应在左右,实验制得的环己烯精品质量低于理论产量,可能的原因是()
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇挥发随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是。
a.用酸性高锰酸钾溶液 b.用溴水 c.测定沸点
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。请回答该实验中的问题。
(1)写出该反应的反应方程式 。
。
(2)圆底烧瓶中盛装的是水,该装置受热后的主要作用是;烧瓶底部放置了几片碎瓷片,其作用是 。
(3)试管中收集气体是,如果要在A处玻璃管处点燃该气体,则必须对该气体进行。
(1)实验室常用氯化铵固体跟氢氧化钙粉末混合加热制取氨气,该反应的化 学方程式为;
学方程式为;
(2)实验室制取氨气时应用的发生装置是下图中的(填标号),收集装置是
(填标号),选用该收集装置而不用图中另外两个收集装置的原因是。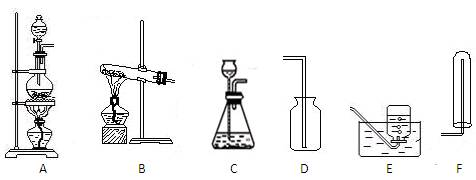
(3)实验室可用C装置制取的气体是(任答一种),该反应的化学方程式为。
为除去粗盐中的Ca2+. Mg2+. SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)
(1)第④步中,写出相应的离子方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)
; _______________________________
(2)在(1)中应使用除杂试剂的化学式__________,在(2)中的操作名称是_______。
(3)从实验设计方案优化的角度分析步骤 ②和④可否颠倒_
②和④可否颠倒_ ___________(填“是”或“否”,如果“否”,请说明理由。___________________________________________;
___________(填“是”或“否”,如果“否”,请说明理由。___________________________________________;
步骤③和④可否颠倒___________。
(4)若先用盐酸再进行 操作⑤,将对实验
操作⑤,将对实验 结果产生影响,其原因是:
结果产生影响,其原因是:
(5)判断BaCl2已过量的方法是