20℃时,饱和KCl溶液的密度为1.174 g·cm-3,物质的量浓度为4.0mol·L-1,则下列说法不正确的是
| A.30℃时,饱和KCl溶液的浓度大于4.0mol·L-1 |
| B.30℃时,饱和KCl溶液的密度大于1.174 g·cm-3 |
| C.将此溶液蒸发部分水,再恢复到20℃时,溶液的浓度大于4.0mol·L-1 |
| D.将此溶液蒸发部分水,再恢复到20℃时,溶液的密度仍为1.174 g·cm-3 |
为进行Ⅰ项中的除杂实验(括号内为杂质),请从Ⅱ项中选出一种试剂,从Ⅲ项中选出合适的实验操作方法分离,将标号填在后面的答案栏内。
| Ⅰ除杂实验 |
Ⅱ 试剂 |
Ⅲ 操作方法 |
答案 |
||
| Ⅰ |
Ⅱ |
Ⅲ |
|||
| ①苯(苯甲酸) |
A.饱和Na2CO3溶液 B.溴水 C.NaOH溶液 D.CaO |
a.蒸馏 b.分液 c.洗气 d.过滤 |
① |
||
| ②乙醇(水) |
② |
||||
| ③乙烷(乙烯) |
③ |
||||
| ④乙酸乙酯(乙酸) |
④ |
某有机样品3.1 g完全燃烧,燃烧后的混合物通入过量的澄清石灰水,石灰水共增重7.1g ,经过滤得到10 g沉淀。该有机样品是
| A.乙二醇(C2H6O2) | B.乙醇 |
| C.乙醛 | D.甲烷和丙烷(C3H8)的混合物 |
在一定温度下,容器内某一反应中M、N(均为气态)的物质的量随反应时间的变化曲线如图,下列表述中正确的是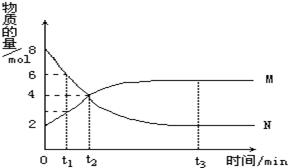
A.反应的化学方程式为:2M N N |
| B.t2时,正逆反应速率相等,达到平衡 |
| C.t3时,正反应速率大于逆反应速率 |
| D.t1时,N的浓度是M浓度的2倍 |
已知下列反应的反应热
(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ,△H1=-870.3kJ/mol
(2)C(s)+O2(g)=CO2(g) ,△H2=-393.5kJ/mol
(3)H2(g)+1/2O2(g)=H2O(l) ,△H3=-285.8kJ/mol
则下列反应的反应热为2C(s)+2H2(g)+O2(g) =CH3COOH(l)
| A.△H=-488.3kJ/mol | B.△H3=-244.15kJ/mol |
| C.△H3=-977.6kJ/mol | D.△H3=+488.3kJ/mol |
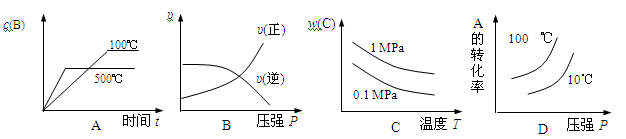
对于可逆反应:2A(g)+B(g)  2C(g) △H<0,下列各图中正确的是
2C(g) △H<0,下列各图中正确的是