某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应中还原产物是_____;若反应过程中转移了0.3mol电子,则氧化产物的质量是____。
(1)实验室中常用加热分解氯酸钾制取氧气,写出反应的化学方程式,并用双线桥法标出电子转移情况:。
(2)实验室制取Cl2的反应方程式之一为: 。
。
被氧化的盐酸占反应盐酸总量的;
当标准状况下有11.2L氯气生成时,该反应的电子转移数为。
(3)已知下列两个氧化还原反应:O2+4HI===2I2+2H2O 及Na2S+I2===2NaI+S,则三种单质的氧化性顺序为:
(4)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:;在以上中性溶液中继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式:。
(5)医疗上常用小苏打治疗胃酸过多,小苏打溶液与盐酸反应的离子方程式为:。
从①渗析、②聚沉、③丁达尔效应、④凝胶、⑤布朗运动、⑥电泳
中选出适当的序号填入下列每小题后面的空格中:
(1)用半透膜把制取的Fe(OH)3胶体中生成的氯化钠分离的方法叫做 。
(2)在肥皂水中透过强光,可见到光带,这种现象称为。
(3)在Fe(OH)3胶体中加入(NH4)2SO4,产生红褐色沉淀,这种现象叫做__________。
(4)在水泥厂和冶金厂常用高压电对气溶胶作用,除去大量烟尘,以减小对空气的污染。这种做法应用的主要原理是_____________。
电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从使用过的腐蚀废液中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤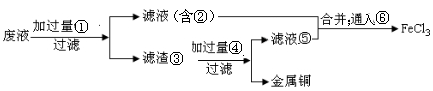
请写出上述实验中加入或生成的有关物质的化学式
①②③④⑥
(2)写出FeCl3溶液与金属铜发生反应的化学方程式
(3)检验腐蚀废液中含有Fe3+的实验操作是
(4)废液加入过量①后,可能发生的离子方程式
(1)有下列物质:①石墨;②银;③氢氧化钠固体;④稀硫酸;⑤熔融氯化钾;⑥醋酸;⑦液态氯化氢;⑧硫酸钡;⑨氨气;⑩蔗糖。
其中能导电的有;属于电解质的有;属于非电解质的有。
(2)实验证明,下面六种物质是一个氧化还原反应的反应物和生成物:FeSO4,Fe2(SO4)3,Fe(NO3)3,NO,HNO3,H2O,在这六种物质中,产物是,还原剂是,被还原的元素是。
研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g)K1∆H1 < 0(I)
NaNO3(s)+ClNO(g)K1∆H1 < 0(I)
2NO(g)+Cl2(g) 2ClNO(g) K2∆H2 < 0(II)
2ClNO(g) K2∆H2 < 0(II)
(1)4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=(用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=(用K1、K2表示)。
(2)为研究不同条件对反应(II)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(II)达到平衡。测得10min内 (ClNO)=7.5×10-3mol•L-1•min-1,则平衡后n(Cl2)=mol,NO的转化率α1=。其它条件保持不变,反应(II)在恒压条件下进行,平衡时NO的转化率α2α1(填“>”“<”或“=”),平衡常数K2(填“增大”“减小”或“不变”)。若要使K2减小,可采用的措施是。
(ClNO)=7.5×10-3mol•L-1•min-1,则平衡后n(Cl2)=mol,NO的转化率α1=。其它条件保持不变,反应(II)在恒压条件下进行,平衡时NO的转化率α2α1(填“>”“<”或“=”),平衡常数K2(填“增大”“减小”或“不变”)。若要使K2减小,可采用的措施是。