2013年,科学家们发明了一种能够给电子设备提供动力的生物电池。该电池包括两个涂覆着酶的电极,它们处于充满空气和少量氢气的槽中。由于气体可以混合从而省去了昂贵的燃料隔离膜,其工作原理如图所示。下列说法正确的是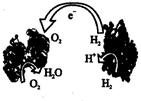
| A.左边为该电池的负极 | B.该电池可在高温环境下使用 |
| C.该电池负极反应为:H2-2e-==2H+ | D.该电池正极反应为:O2+4e-==2O2- |
胶体区别于其它分散系的本质特征是 ()
()
| A.胶体粒子直径在1-100nm之间 | B.胶体粒子带电荷 |
| C.胶体粒子不能穿过半透膜 | D.胶体粒子能够发生布朗运动 |
氧化还原反应在生产、生活中具有广泛的用途。下列生产、生活中的事例不属于氧化还原反应的是()
| A.金属冶炼 | B.燃放鞭炮 | C.食物腐败 | D.点制豆腐 |
A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球.
关闭K2,将等量且少量的NO2通过K1、K3分别充入A、B中,反应开始时,A、B的体积相同。已知:2NO2(g) N2O4(g)△H<0。
N2O4(g)△H<0。
(1)一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是V(A)V(B)(填“<”、“>”或“=”);若打开活塞K2,气球B将(填“变大”、“变小”或“不变”,下同)。
(2)若在A、B中再充入与初始量相等的NO2,则达到平衡时,NO2的转化率α(A)将。
若通入等量的Ne气,则达到平衡时,A中NO2的转化率将,B中NO2的转化率将。
(3)室温时,若A、B都保持体积不变,将A套上一个绝热层,B与外界可以进行热传递,则达到平衡时,中的颜色较深。
(4)若在容器A中充入4.6g的NO2,达到平衡后容器内混合气体的压强为原来的80%,试求出平衡时NO2的转化率(写出计算过程)
工业合成氨与制备硝酸一般可连续生产,流程如下: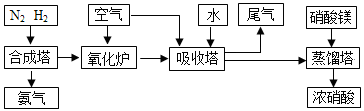
(1)在合成氨的反应中,改变反应条件,会使平衡发生移动。如下图像表示随条件改变,氨气的百分含量的变化趋势。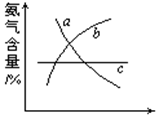
当横坐标为压强时,变化趋势正确的是(选填字母序号)_________,
当横坐标为温度时,变化趋势正确的是(选填字母序号)。
(2)如图所示三个容积相同的容器①、②、③,若起始温度相同,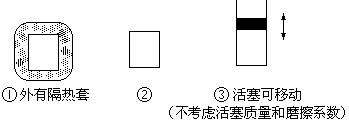
分别向三个容器中充入3mol H2和1mol N2,一定条件下反应,达到平衡时各容器中NH3物质的百分含量由小到大的顺序为(填容器编号)
有如下化学反应:2A(g)+B(g) 2C(g),△H<0。
2C(g),△H<0。
(1)若将4 mol A和2 mol B在2 L的容器中混合,经2 s后测得C的浓度为0.6 mol/L,用物质A表示的平均反应速率为____________________________;2s时物质B的浓度为____________________;
(2)若将4 mol A和2 mol B加入体积不变的容器中,一定温度下达到平衡状态,测得气体总物质的量为4.2 mol。此时,混合气体中C的体积分数为_____________;若再通入少量B气体,体系中A的物质的量_________(填“增大”、“减小”或“不变”),若要使A的物质的量再达到与原平衡状态相同,可采取的措施有_。(填一种措施即可)
(3)下图是一定条件下该反应过程中,体系内各物质浓度的变化情况。t2时曲线发生变化的原因是_______________________________ ,若在t4时将B的浓度增大0.l mol·L-1,在t5时刻到达新平衡。请在图中画出各物质浓度的变化情况。