限用硝酸、硫酸、盐酸、醋酸、钠盐、钾盐、钡盐相互反应,符合离子方程式:
2H++SO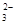 ===H2O+SO2↑的化学方程式个数有
===H2O+SO2↑的化学方程式个数有
| A.4 | B.5 | C.8 | D.12 |
50℃时,下列各溶液中,离子的物质的量浓度关系正确的是
| A.饱和纯碱(Na2CO3)溶液中:c(Na+)=2c(CO32-) |
| B.pH=4的醋酸中:c(H+)=1.0×10-4mol·L-1 |
| C.0.10mol/L醋酸钠溶液中:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| D.pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol·L-1 |
下列实验装置(固定装置略去)和操作正确的是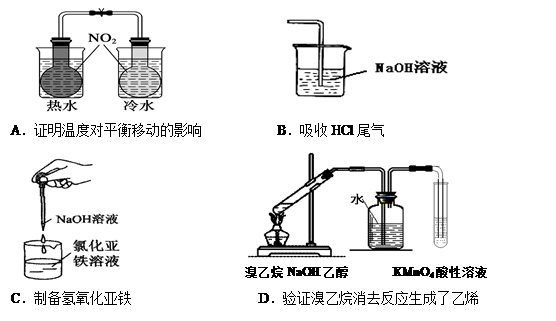
下列陈述Ⅰ、Ⅱ都正确并且有因果关系的是
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
浓硫酸有强氧化性 |
浓硫酸不能用于干燥H2S和HI气体 |
| B |
NH4Cl为强酸弱碱盐 |
用加热法除去NaCl中的NH4Cl |
| C |
溶解度:CaCO3<Ca(HCO3)2 |
溶解度:Na2CO3<NaHCO3 |
| D |
SiO2是两性氧化物 |
SiO2能与NaOH溶液和氢氟酸反应 |
某同学通过系列实验探究Mg及其化合物的性质,操作正确且能达到目的的是
| A.将水加入浓硫酸中得到稀硫酸,置镁条于其中探究Mg的活泼性 |
| B.将NaOH溶液缓慢滴入MgSO4溶液中,观察Mg(OH)2沉淀的生成 |
| C.将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀 |
| D.将Mg(OH)2沉淀转入蒸发皿中,加足量稀盐酸,加热蒸干得无水MgCl2固体 |
能在溶液中大量共存的一组离子是
| A.NH4+、Ca2+、SO42-、CO32- | B.Fe3+、H+、I-、HCO3- |
| C.K+、Na+、H+、NO3-、MnO4- | D.Al3+、Mg2+、SO42-、CO32- |