(15分)某研究小组设计如下装置分离CO和CO2的混合气体并探究CO还原氧化铜的产物和过氧化钠的性质。已知氯化钯(PdCl2)溶液遇CO气体会产生黑色沉淀(金属单质)。夹持装置未画出。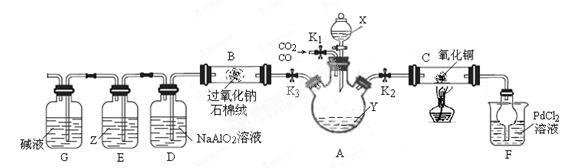
(题9图)
(1)试剂X、Y的焰色反应均呈黄色,则X、Y可能是 、 .
(2)连接装置、检验气密性并装好药品后,关闭分液漏斗活塞和K3,打开K1、K2,分离出CO,当观察到 现象时,可对C装置进行加热操作,反应产物为红色固体。
(3)查询资料获得以下信息:①Cu2O为红色固体;②常温下,Cu2+在溶液中稳定,Cu+易在酸性条件下发生反应:2Cu+ =Cu2++Cu。
甲、乙两组同学取上述红色固体(用M代表)进行实验,探究其成分:
| 组别 |
实验操作 |
实验现象或数据 |
结 论 |
| 甲 |
① 向a g M中加入一定量稀硫酸,充分搅拌; ② 继续滴加稀硫酸至过量, 充分反应. |
①固体明显减少; ②仍然有一定量固体,溶液呈蓝色 |
①M中一定有Cu2O; ②M中一定有Cu. |
| 乙 |
将甲实验后所得溶液过滤 将滤渣洗涤、干燥、称量 |
滤渣质量为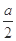 g g |
M为Cu和Cu2O的混合物 |
(i)乙组同学认为甲组同学所得结论不可靠,其理由是 .
(ii)甲组同学配合乙组同学进行了计算,认为乙组同学的结论是正确的,并得出M中Cu和Cu2O的物质的量之比是 .
(4)C装置反应结束后,欲从混合气体中分离出CO2,需进行的主要操作是 .实验过程中D装置产生白色沉淀的离子方程式为 .
(5)Z试剂为混有KI的苯溶液,则E装置中可能产生的现象是 .
硫代硫酸钠(Na2S2O3)俗称大苏打,照相业中用作定影剂。Na2S2O3易溶于水,在酸性溶液中与酸反应有单质硫和SO2生成。
(1)Na2S2O3溶液与稀硫酸混合反应可用于探究外界条件对反应速率的影响,完成有关的实验设计表(已知各溶液体积均为5 mL):
| 实验编号 |
T/K |
c(Na2S2O3)/ mol·L-1 |
c(H2SO4)/ mol·L-1 |
实验目的 |
| ① |
298 |
0.1 |
0.1 |
实验①和②探究温度对该反应速率的影响;实验①、③和④探究反应物浓度对该反应速率的影响 |
| ② |
308 |
|||
| ③ |
0.2 |
|||
| ④ |
0.1 |
(2)Na2S2O3还具有很强的还原性,Na2S2O3溶液与足量氯水反应的化学方程式为:
________(提示:S元素被氧化为SO)。
(3)现有一瓶Na2S2O3固体,可能含有Na2SO4固体,请设计实验验证,写出实验步骤、预期现象和结论。限选试剂: 1 mol·L-1 H2SO4、1 mol·L-1 HNO3、1 mol·L-1 HCl、1 mol·L-1 NaOH、0.1 mol·L-1 BaCl2、0.01 mol·L-1 KMnO4、蒸馏水。
| 实验步骤 |
预期现象和结论 |
| 步骤1:取少量固体于试管中,加蒸馏水溶解 |
|
| 步骤2: |
|
| 步骤3: |
菱镁矿是碱性耐火材料的主要原料,其主要的化学成分是:MgCO3,同时含有杂质:SiO2、Al2O3、Fe2O3、CaO等;目前以菱镁矿为主要原料制备MgSO4的方法如下: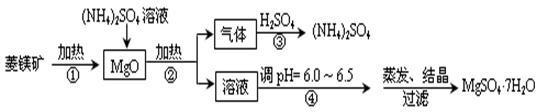
已知:①常温下,Fe3+、Al3+、Mg2+开始形成氢氧化物沉淀和沉淀完全时的pH值如下:
| Fe3+ |
Al3+ |
Mg2+ |
|
| 开始沉淀 |
2.1 |
3.7 |
9.0 |
| 沉淀完全 |
3.2 |
5.2 |
12.4 |
②MgSO4·7H2O在70~80℃时失去3个结晶水,300℃时失去全部的结晶水;
(1)用平衡原理解释:菱镁矿粉粹后加热生成的氧化镁可以溶解在硫酸铵溶液中的原因 。
(2)在该工业流程中,可以循环使用的物质是。
(3)步骤③中氨气和硫酸恰好完全反应,取此时所得的溶液10.00mL配成250mL溶液,配制溶液过程中除烧杯、玻璃棒、胶头滴管、酸式滴定管外,还需要的玻璃仪器有:;经检测所配制的溶液pH=1,c(SO42ˉ)=1.05mol/L,试求算所配制溶液中NH4+ 水解的平衡常数K(写计算过程,计算结果保留三位有效数字)。
(4)在加热条件下杂质中的三氧化二铁溶于硫酸铵的离子反应方程式是:
。
(5)蒸发结晶过程中需要使用60~70℃水浴加热方式,其原因是。
已知:将KI、盐酸、试剂X和淀粉四种溶液混合,无反应发生。
①向其中滴加双氧水,发生反应:H2O2+2H++2Iˉ=2H2O+I2;
②生成的I2立即与试剂X反应,当试剂X消耗完后,生成的 I2才会遇淀粉变蓝因此,根据试剂X的量、滴入双氧水至溶液变蓝所需的时间,即可推算:H2O2+2H++2Iˉ= 2H2O+I2的反应速率。
下表为某同学依据上述原理设计的实验及实验记录(各实验均在室温条件下进行):
| 编号 |
往烧杯中加入的试剂及其用量(mL) |
催化剂 |
开始变蓝时间(min) |
||||
| 0.1 mol·Lˉ1 KI溶液 |
H2O |
0.01 mol·Lˉ1 X溶液 |
0.1mol·Lˉ1 双氧水 |
1mol·L1 稀盐酸 |
|||
| 1 |
20.0 |
10.0 |
10.0 |
20.0 |
20.0 |
无 |
1.4 |
| 2 |
20.0 |
m |
10.0 |
10.0 |
n |
无 |
2.8 |
| 3 |
10.0 |
20.0 |
10.0 |
20.0 |
20.0 |
无 |
2.8 |
| 4 |
20.0 |
10.0 |
10.0 |
20.0 |
20.0 |
5滴Fe2(SO4)3 |
0.6 |
(1)已知:实验1、2的目的是探究H2O2浓度对H2O2+2H++2Iˉ= 2H2O+I2反应速率的影响。实验2中m=,n=。
(2)已知,I2与X完全反应时,两者物质的量之比为1∶2。按表格中的X和KI的加入量,加入V(H2O2)>________,才确保看到蓝色。
(3)实验1,浓度c(X)~ t的变化曲线如图,若保持其它条件不变,请在答题卡坐标图中,分别画出实验3、实验4,c(X) ~ t的变化曲线图(进行相应的标注)。
(4)实验4表明:硫酸铁能提高反应速率。催化剂能加快反应速率是因为催化剂(填“提高”或“降低”)了反应活化能。
(5)环境友好型铝—碘电池已研制成功,已知电池总反应为:2Al(s)+3I2(s)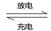 2AlI3(s)。含Iˉ传导有机晶体合成物作为电解质,该电池负极的电极反应为:________________________,充电时Al连接电源的___________极。
2AlI3(s)。含Iˉ传导有机晶体合成物作为电解质,该电池负极的电极反应为:________________________,充电时Al连接电源的___________极。
(6)已知:N2H4(l) +2H2O2(l)= N2(g)+4H2O(g)△H1= -640kJ/mol
H2O(l)=H2O(g)△H2=+44.0kJ/mol
则0.25mol 液态肼与液态双氧水反应生成液态水时放出的热量是。
1-乙氧基萘是一种无色液体,密度比水大,不溶于水,易溶于乙醇,熔点5.5℃,沸点267℃。1-萘酚(性质与苯酚相似)熔点96℃,沸点278℃,微溶于水,易溶于乙醇,乙醇的沸点为78.5℃。1-乙氧基萘常用作香料,也可合成其他香料。实验室制备1-乙氧基萘的过程如下: +C2H5OH
+C2H5OH
 +H2O
+H2O
1-萘酚 1-乙氧基萘
(1)将72g1-萘酚溶于100mL无水乙醇中,加入5mL浓硫酸混合。将混合液置于如图所示的容器中加热充分反应。实验中使用过量乙醇的原因是。烧瓶上连接长直玻璃管的主要作用是。 
(2)反应结束,将烧瓶中的液体倒入冷水中,经处理得到有机层。为提纯产物有以下四步操作:①蒸馏;②水洗并分液;③用10%的NaOH溶液碱洗并分液;④用无水氯化钙干燥并过滤。正确的顺序是(填序号)。
A.③②④① B.①②③④ C.②①③④
(3)实验测得1-乙氧基萘的产量与反应时间、温度的变化如图所示,时间延长、温度升高,1-乙氧基萘的产量下降的原因可能是、。
(4)某同学推测经提纯的产品可能还含有1-萘酚、乙醇、硫酸和水等杂质,设计了如下方案进行检验,请在答题卡上完成表中内容。
| 实验目的 |
实验操作 |
预期现象和结论 |
| ①用金属钠检验1-乙氧基萘是否纯净 |
取少量经提纯的产品于试管A中,加入金属钠 |
若,则产品纯净; 若,则产品不纯。 |
| ②检验经提纯的产品是否含有1-萘酚 |
若,则含有1-萘酚; 若,则不含1-萘酚。 |
如图是现今常规生产发烟硫酸和硫酸的流程图
(1)在④处二氧化硫被催化成三氧化硫,④的设备名称是。该处发生反应的方程式为。为提高三氧化硫的产率,该处应采用(填“等温过程”或“绝热过程”)为宜。
(2)在⑦处进行二次催化处理的原因是。
(3)⑤处气体混合物主要是氮气和三氧化硫。此时气体经过⑥后不立即进入⑦是因为
(4)20%的发烟硫酸(SO3的质量分数为20%)1吨需加水吨(保留2位有效数字)才能配置成98%的成品硫酸。
(5)在②处发生1500℃的“不完全燃烧”,即先混入少量干燥空气,然后在③处于700℃下再继续燃烧。试说明为何这种燃烧方式对环境保护是有利的?。