下列说法正确的是
| A.常温下物质的量浓度相等的①(NH4)2CO3 ②(NH4)2SO4③ (NH4)2Fe(SO4)2三种溶液中水的电离程度:③>②>① |
B.常温下醋酸和醋酸钠混合溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示,当pH=4.5溶液中:c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-)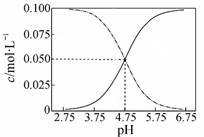 |
| C.向Ca(OH)2溶液中加入过量的NaHCO3溶液: Ca2++2HCO3-+2OH-→ CO32-+CaCO3↓+2H2O |
| D.25°C时,HCN溶液的电离平衡常数(Ka)与NaCN溶液的水解平衡常数(K)存在如下关系: Kw ·K = Ka |
根据下列事实所作出的结论正确的是
| 选项 |
事实 |
结论 |
| A |
完全燃烧产物是CO2和H2O的物质 |
一定只含C、H元素 |
| B |
灼烧棉织品、羊毛衫和涤纶衣物 |
有烧焦羽毛气味的是羊毛衫 |
| C |
在淀粉溶液中加入市售的加碘食盐不出现蓝色 |
说明此盐一定不含碘 |
| D |
甲乙两种有机物,相对分子质量相同,结构不同 |
甲和乙一定是同分异构体 |
下列各组混合物中,以任意比例混合,只要总质量固定,经充分燃烧后产生CO2的量为一恒定值的是
| A.甲醛和甲酸乙酯 | B.乙醇和乙酸 |
| C.丙烯和丙烷 | D.乙炔和苯蒸气 |
莽草酸可用于合成药物达菲,结构简式如图,关于莽草酸的说法不正确的是
| A.分子式为C7H10O5 |
| B.分子中含有3种官能团 |
| C.可发生加成反应和酯化反应 |
| D.在水溶液中羧基和羟基均能电离出H+而使溶液显酸性 |
下列生产、生活情境都涉及能量转化和利用,其中不发生化学变化的是
氢氧燃料电池是将H2和O2通入电池,穿过浸入20%—40%的KOH溶液的多孔碳电极,其电极反应式分别为:2H2+4OH--4e-= 4H2O和O2+2H2O+4e-= 4OH-,下列不正确的是
| A.氢氧燃料电池属于环境友好电池 |
| B.通O2的极是正极,通入H2的极是负极 |
| C.工作一段时间后KOH溶液的溶质质量分数增大 |
| D.工作时溶液中的OH-向负极作定向移动 |