常用解热镇痛药—扑热息痛的结构简式为 HO—C6H4—NHCOCH3(C6H4表示苯环)。 对它的叙述有:①能与NaHCO3溶液反应;②能发生水解反应;③不能与浓溴水发生取代反应;④遇三氯化铁溶液显紫色。其中正确的是
| A.①和② | B.①和④ | C.②和③ | D.②和④ |
鉴别甲烷、一氧化碳、氢气三种无色气体的方法,是将它们分别
| A.先后通入溴水和澄清石灰水中 |
| B.点燃后罩上内壁涂有澄清石灰水的烧杯 |
| C.点燃后罩上内壁涂有澄清石灰水的烧杯,通入溴水 |
| D.点燃,先后罩上干燥的冷烧杯和内壁涂有澄清石灰水的烧杯 |
下列各组材料中,不能组成原电池的是
| A |
B |
C |
D |
|
| 两极材料 |
锌片、铜片 |
锌片、石墨 |
铜片、银片 |
铁片、铜片 |
| 插入溶液 |
乙醇溶液 |
硫酸溶液 |
硝酸银溶液 |
稀盐酸 |
下列反应中属于氧化还原反应,但水既不做氧化剂,又不做还原剂的是
| A.ICl+H2O=HCl+HIO | B.2K+2H2O=2KOH+H2↑ |
| C.2F2+2H2O=4HF+O2 | D.2Na2O2+2H2O=4NaOH+O2 |
下列实验中,不能观察到明显变化的是
| A.把溴水滴加到氯化亚铁溶液中 |
| B.CO2通入CaCl2溶液中 |
| C.向饱和Na2CO3溶液中通入足量CO2 |
| D.把少量氯气通入到淀粉碘化钾溶液中 |
下列有关化学用语使用正确的是
A.CH4分子的比例模型: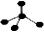 |
B.NH3的电子式: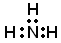 |
C.硫离子的离子结构示意图: |
D.聚乙烯的结构简式为: 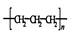 |