如将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2即构成甲烷燃料电池。已知通入甲烷的一极,其电极反应为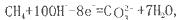 ,下列叙述正确的是
,下列叙述正确的是
| A.通入甲烷的一极为正极 |
| B.通入氧气的一极发生氧化反应 |
C.该电池总反应为 |
| D.该电池在工作时,溶液中的阴离子向正极移动 |
有一种二肽的化学式是C8H14N2O5,水解后得到丙氨酸和另一氨基酸X,X的化学式是( )
| A.C5H7NO3 | B.C5H9NO4 | C.C5H11NO5 | D.C5H7NO4 |
葡萄糖的分子式为C6H12O6,通过缩聚反应把10个葡萄糖分子连接起来所形成的链状化合物的分子式为( )
| A.C60H120O60 | B.C60H100O52 | C.C60H102O51 | D.C60H112O51 |
1 mol某有机物在稀硫酸作用下,水解生成2 mol相同的物质。下列物质中:
①蔗糖 ②麦芽糖 ③淀粉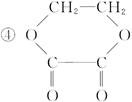
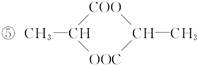
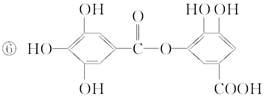
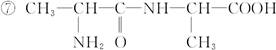
符合题意的物质可能是( )
| A.①②⑤⑦ | B.④⑤⑦ | C.②⑤⑥⑦ | D.①④⑤⑥ |
关于生物体内氨基酸的叙述错误的是( )
A.构成蛋白质的氨基酸分子的结构通式是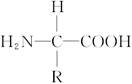 |
| B.人体内氨基酸的分解代谢终产物是水、二氧化碳和尿素 |
| C.人体内所有氨基酸均可以互相转化 |
| D.两个氨基酸通过脱水缩合形成二肽 |
有关食品添加剂的下列说法正确的是( )
| A.食盐加碘,碘元素质量分数越高,说明食盐的质量越高 |
| B.可供糖尿病人食用的木糖醇是一种单糖 |
| C.苯甲酸钠是常用的食品防腐剂 |
| D.腌制肉食制品使用的硝酸盐或亚硝酸盐食品添加剂即使不超标准,也对人体造成极大伤害 |