(共10分)丙烯醇(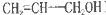 )是一种无色有刺激性气味的液体,是重要的有机合成原料。请回答:
)是一种无色有刺激性气味的液体,是重要的有机合成原料。请回答:
(1)丙烯醇的分子式为__________;丙烯醇中含有的官能团的名称是__________。
(2)0.3mol丙烯醇与足量金属钠反应,能生成标准状况下的氢气_________ L。
(3)写出丙烯醇与溴水反应的化学方程式____________________________
反应类型为____________________
(4)丙烯醇与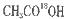 发生酯化反应的化方程式为:________________________________酯化反应生成的产物在一定条件下可以发生加聚反应得到高分子化舍物,其结构简式为____________________________。
发生酯化反应的化方程式为:________________________________酯化反应生成的产物在一定条件下可以发生加聚反应得到高分子化舍物,其结构简式为____________________________。
苯酚是一种重要的化工原料。以苯酚为主要起始原料,经下列反应可制得香料M和高分子化合物N。(部分产物及反应条件已略去)
(1)B的官能团名称_____________。苯酚与浓溴水反应生成白色沉淀,可用于苯酚的定性检验和定量测定,反应的化学方程式为。
(2)已知C的分子式为C5H12O,C能与金属Na反应,C分子中有3中不同化学环境的氢原子,则M的结构简式为。
(3)生成N的反应的化学方程式,反应类为。
(4)以苯酚为基础原料也可以合成防腐剂F,已知F的相对分子质量为152,其中氧元素的质量分数为31.58%,F完全燃烧只生成CO2和H2O,则F的分子式是;
已知F具有如下结构特征:
①分子结构中含有苯环,能与NaHCO3溶液反应,但不能发生水解反应;
②分子结构中不存在“-O-O-”的连接方式。
符合上述条件的F的同分异构体有种,其中核磁共振氢谱显示其分子中含有4种不同的氢原子的是(写结构简式)
I、铝是地壳中含量最高的金属元素,其单质及其合金在生产生活中的应用十分广泛。
(1)金属铝的生产是以Al2O3为原料,与冰晶石(Na3AlF6)在熔融状态下进行电解,则化学方程式为:.其电极均由石墨材料做成,则电解时不断消耗的电极是;(填“阴极”或“阳极”)。
(2)对铝制品进行抗腐蚀处理,可延长其使用寿命.以处理过的铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极反应式为;
(3)铝电池性能优越,Al-Ag2O电池可用作水下动力电源,化学反应为2Al+3Ag2O+2NaOH+3H2O═2Na[Al(OH)4]+6Ag,则负极的电极反应式为,正极附近溶液的pH(填变大、不变或变小)。
II、氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)图是在一定温度和压强下N2和H2反应生成1molNH3过程中能量变化示意图,请写出合成氨的热化学反应方程:(△H的数值用含字母a、b的代数式表示)。
(2)工业合成氨反应如下,
在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中,反应达到平衡后,改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是。
| A.增大压强 | B.增大反应物的浓度 | C.使用催化剂 | D.降低温度 |
Ⅲ、铁及其化合物在生活、生产中有广泛应用.请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为:
有3molFeS2参加反应,转移mol电子。
(2)氯化铁溶液称为化学试剂中的“多面手”,写出SO2通入氯化铁溶液中反应的离子方程式。
氮化硼(BN)是一种重要的功能陶瓷材料.以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示
请回答下列问题:
(1)由B2O3制备BF3、BN的化学方程式依次是、;
(2)基态B原子的电子排布式为;B和N相比,电负性较大的是
,BN中B元素的化合价为;
(3)在BF3分子中,F-B-F的键角是,B原子的杂化轨道类型为
,BF3和过量NaF作用可生成NaBF4,BF4-的立体结构为;
(4)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为,层间作用力为;
(5)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,立方氮化硼晶胞中含有个氮原子、个硼原子,立方氮化硼的密度是g•cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)
某有机物X(C12H13O6Br)的分子中多种官能团,其结构简式为:
(其中Ⅰ、Ⅱ未知部分),已知X可以发生如图所示的转化
已知向X、E的水溶液中滴入FeCl3溶液均发生显色反应,E的核磁共振氢谱图中只有两个峰;G、M都能与NaHCO3溶液反应。
(1)由B转化成D的化学方程式是;
(2)G分子所含官能团名称是;
(3)E的结构简式是;
(4)F与G互为同分异构体,F的分子中只羧基、羟基和醛基三种,且同一个碳原子上不能同时连有两个羟基.则F的分子结构有种
废旧锂离子池的正极材料(主要含有LiCoO2及少量的Al、Fe等)可用于回收钴、锂,工艺流程如下:
(1)在上述溶解过程中,S2O32-被氧化成SO42-,LiCoO2在溶解过程中发生反应的化学方程式为,还原产物是。
(2)在上述除杂过程中,通入空气的作用是废渣的主要成分是。
(3)“沉淀钴”和“沉淀锂”的离子方程式分别为。
(4)除了废渣可以回收利用外,本工艺还可回收的副产品是。