下列实验或操作能达到实验目的的是

医疗上的血液透析原理同胶体的渗析类似。透析时,病人的血液通过浸在透析液中的透析膜进行循环和透析。血液中,蛋白质和血细胞不能通过透析膜,血液中的毒性物质可以透过,由此可以判断
| A.蛋白质、血细胞的粒子直径大于毒性物质的直径 |
| B.蛋白质以分子形式存在,毒性物质以离子形式存在 |
| C.蛋白质、血细胞不溶于水,毒性物质可溶于水 |
| D.蛋白质、血细胞不能透过滤纸,毒性物质可以透过滤纸 |
环境污染已成为人类面临的重大威胁之一,下列选项属于海洋污染的是
| A.酸雨 | B.白色污染 | C.温室效应 | D.赤潮 |
在强酸性的无色透明溶液中,不能大量共存的离子组是( )
A.Al3+、Ag+、 、Cl- 、Cl- |
B.Mg2+、 、 、 、Cl- 、Cl- |
| C.Ba2+、K+、S2-、Cl- | D.Zn2+、Na+、 、 、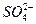 |
下列离子方程式正确的是()
| A.澄清石灰水中通少量CO2 Ca(OH)2+CO2====CaCO3↓+H2O |
| B.石灰乳中加稀盐酸 OH-+H+====H2O |
C.碳酸氢钠溶液中加稀H2SO4 +H+====CO2↑+H2O +H+====CO2↑+H2O |
| D.铁加稀盐酸 2Fe+6H+====2Fe3++3H2↑ |
判断下列说法是否正确:
(1)Ba2++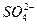 ====BaSO4↓,表示所有钡盐与硫酸或硫酸盐的反应()
====BaSO4↓,表示所有钡盐与硫酸或硫酸盐的反应()
(2)2H++ ====H2O+CO2↑,表示所有酸与碳酸盐的反应()
====H2O+CO2↑,表示所有酸与碳酸盐的反应()