下列溶液中的Cl-浓度与100mL 0.5 mol·L-1AlCl3溶液中Cl-的浓度相等的是( )
| A.50mL 1.5 mol·L-1的KCl溶液 |
| B.50mL 0.5 mol·L-1的FeCl2溶液 |
| C.100mL 1 mol·L-1的MgCl2溶液 |
| D.450mL 0.5 mol·L-1的NaCl溶液 |
用下列装置进行的实验,不能达到相应实验目的的是 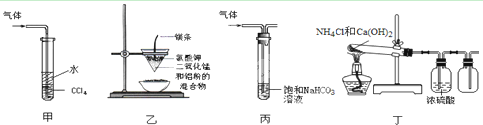
| A.装置甲:吸收尾气HCl | B.装置乙:制取金属锰 |
| C.装置丙:洗气除去CO2中的SO2 | D.装置丁:实验室制取NH3 |
分类是重要的科学研究方法,下列物质归类不正确的是
| A.电解质:明矾、氯气、冰醋酸、硫酸钡 |
| B.化合物:干冰、烧碱、冰水混合物、胆矾 |
| C.混合物:铝热剂、矿泉水、水玻璃、漂白粉 |
| D.同素异形体:C60、C70、金刚石 |
用NA表示阿伏加德罗常数的值,下列叙述中正确的是
| A.1mol氯气参加氧化还原反应,转移的电子数一定为2NA |
| B.在同温同压下,相同体积的任何气体单质所含的原子数目相同 |
| C.14 g乙烯和丙烯的混合物中总原子数为3NA个 |
| D.含2molH2SO4的浓硫酸与足量铜片在加热条件下反应,一定能产生NA个SO2气体分子 |
今年七、八月份,我市经历了“史上最热”的夏天,为了缓解高温干旱的天气,市气象部门曾多次进行了人工降雨作业,下列物质中能用作人工降雨剂的是
| A.冰晶石 | B.二氧化碳气体 | C.重晶石 | D.碘化银 |
700℃时,在容积为2 L的密闭容器中发生反应CO(g) + H2O(g) CO2(g) + H2(g),部分数据见下表(表中t2>t1):
CO2(g) + H2(g),部分数据见下表(表中t2>t1):
| 反应时间/min |
n(CO)/mol |
n(H2O)/mol |
n(CO2)/mol |
n(H2)/mol |
| 0 |
1.20 |
0.60 |
0 |
0 |
| t1 |
0.80 |
|||
| t2 |
0.20 |
下列说法正确的是
A.反应在t1 min内的反应速率为v(H2)=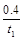 mol·L-1·min-1
mol·L-1·min-1
B.保持其他条件不变,起始时向容器中充入0.60 mol CO和1.20 mol H2O,达到平衡时n(CO2)="0.40" mol
C.保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数减小
D.温度升高至800℃,上述反应的平衡常数为0.64,则正反应为吸热反应