下列化学反应的离子方程式书写正确的是( )
| A.钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
| B.小苏打与醋酸反应:HCO3—+H+==CO2↑+H2O |
C.氯气与水反应:Cl2 +H2O 2H+ + Cl—+ ClO— 2H+ + Cl—+ ClO— |
| D.氯化铝溶液与过量氨水反应:3NH3•H2O+ Al3+ =Al(OH)3↓+3NH4+ |
反应A+B →C分两步进行:①A+B→X,②X →C,反应过程中能量变化如图所示,E1表示反应A+ B→X的活化能。下列有关叙述正确的是()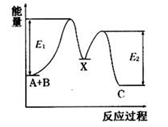
| A.E2表示反应X→C的活化能 |
| B.X是反应A+B→C的催化剂 |
| C.反应A+B→C的△H<0 |
| D.加入催化剂可改变反应A+B→C的焓变 |
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是()
| A.装置①常用于分离互不相溶的液体混合物 |
| B.装置②可用于吸收氨气,且能够防止倒吸 |
| C.装置③可用于制备少量NH3 |
| D.装置④可用于收集O2 |
下列离子方程式正确的是()
| A.0.01mol/L NH4Al(SO4)2溶液与0.02mol/L Ba(OH)2溶液等体积混合 NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O |
| B.FeCl2酸性溶液放在空气中变质:2Fe2++4H++O2===2Fe3++2H2O |
| C.用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ |
D.电解MgCl2水溶液的离子方程式:2Cl-+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
下列叙述不正确的是()
①热稳定性:H2O>HF>H2S
②熔点:Al>Na>K
③第ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤沸点:NH3<PH3<AsH3
⑥已知2H2(g)+O2(g)=2H2O(l) △H=﹣571kJ·mol﹣1,则氢气的燃烧热为285.5kJ·mol﹣1
⑦因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,所以非金属性:P>N
A.②④⑥ B.①③⑤⑦ C.②④⑥⑦ D.①⑤⑥⑦
某溶液中可能含有Na+、Fe2+、Br-、CO32-、I-、SO32-六种离子中的几种。①在该溶液中滴加足量氯水后,有气泡产生、溶液呈橙黄色;②向呈橙黄色的溶液中加入BaCl2溶液时无沉淀生成;③向淀粉溶液中滴加橙黄色溶液未变蓝色。根据上述实验事实推断,在该溶液中肯定存在的离子组是()
| A.Na+、Br-、CO32- | B.Na+、 I-、SO32- |
| C.Fe2+、I-、SO32- | D.Fe2+、Br-、CO32- |