根据下图所示的装置回答问题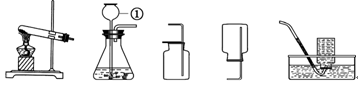
A B C D E
(1)写出标号①的仪器名称_____________。
(2)氨气(NH3)是一种无色有刺激性气味,极易溶于水的气体。实验室常用氯化铵晶体和氢氧化钙粉末混合加热来制取氨气。写出制取氨气的化学方程式___________;选取上述_______(填字母)作为制取氨气的发生装置; 收集氨气只能选用的装置为_______(填字母),其原因是____________________。
某奶制品的部分营养成分如下表所示。
| 项目 |
每100 mL |
| 蛋白质 |
3.4 g |
| 脂肪 |
3.9 g |
| 糖类 |
5.1 g |
| 钠 |
60 mg |
| 钙 |
110 mg |
(1)人体必需六大基本营养素,表中没有标示的基本营养素是___________和___________。
(2)奶制品中含有丰富的钙______(填“单质”或“元素”),人体每日要摄取足够量的钙,否则会导致______(填字母序号)。
A.贫血症 B.坏血病 C.夜盲症 D.骨质疏松
(3)下列是奶制品常用的四种包装,其中所使用的主要材料属于有机合成材料的是______(填字母序号)。
A.铁罐B.纸盒 C.塑料瓶 D.玻璃瓶
用化学用语填空:
(1)钾元素:_________;
(2)镁离子:____;
(3)硝酸根离子:______;
(4)2个水分子:______;
(5)碳酸:______;
(6)NO中N的化合价:___。
下图是实验室制取气体的装置图,回答下列问题(装置选择用序号填写):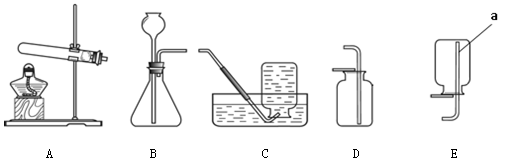
(1)实验仪器a的名称是。
(2)用高锰酸钾制取氧气时,反应的化学方程式为,若要收集干燥的氧气,应选用的收集装置是。
(3)用大理石和稀盐酸制取二氧化碳时,所选用的发生装置是,
反应的化学方程式为。
(8分)水是我们熟悉的物质,通过学习化学和关注新闻报道以后,我们对水有了一些新的认识。
(1)知道了水的微观结构。构成水的粒子表示为(填序号)。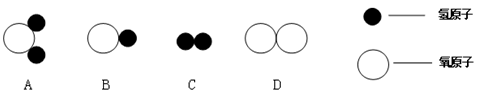
(2)懂得爱护水资源。爱惜水的正确做法是(填序号)
A.右江水量充足,沿岸居民不须节约用水 B.生活污水可任意排放
C.用工业废水直接浇灌农田 D.加强河道管理,保证水质
(3)认识了水的化学性质。氢化钙(CaH2)固体可用于登山队员的能源提供剂,它和水反应生成氢氧化钙和氢气,反应的化学方程式为。
(4)认识了水的用途
①在粗盐提纯中:水做;过滤时玻璃棒的作用是。
②今年“世界水日”的主题是:水与能源。世界能源的大约20%来自水力发电(简称水电)。
水电是一种(填“可再生”或“不可再生”)能源。发展水电的优点是(填序号)。
A.可减缓化石能源的消耗
B.水力发电产生大量的温室气体
C.建水坝淹没土地
D.进行高成本的库区移民
下图是是甲、乙两种固体物质的溶解度曲线,请你回答下列问题: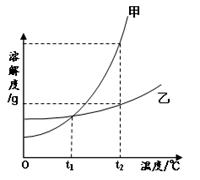
(1)℃时,甲、乙两种物质的溶解度相等;
(2)若固体甲中含有少量乙时,可用方法提纯甲(填“蒸发结晶”或“冷却结晶”);
(3)溶解度受温度影响比较大的物质是;
(4)t2℃时,用等质量的甲、乙两种物质配制甲、乙的饱和溶液需要水的质量:甲乙(填“>”“<”或“=”)