二十一世纪是海洋开发与利用的世纪,我市实施黄蓝两大国家战略形成新的发展格局,海洋化学资源的综合利用将是重点发展领域之一。
(1)海水晒盐:将海水引入蒸发池,经日晒蒸发到一定程度时,导入结晶池,继续日晒,海水就会成为食盐的饱和溶液,再晒就会逐渐析出粗盐,剩余的液体称为母液(也称卤水)。
1L海水在逐渐浓缩过程中不断析出的盐的种类和质量(单位:
)关系如下表所示:
| 海水密度(
) |
||||
| 1.20 |
0.91 |
|||
| 1.21 |
0.05 |
3.26 |
0.004 |
0.008 |
| 1.22 |
0.015 |
9.65 |
0.01 |
0.04 |
| 1.26 |
0.01 |
2.64 |
0.02 |
0.02 |
| 1.31 |
1.40 |
0.54 |
0.03 |
I、海水晒盐是(选填"物理"或"化学")变化,包含蒸发、等过程。
II、若得到纯度较高的粗盐和含浓度较高的卤水,卤水的密度应控制在什么范围,原因是。
(2)海水制镁:海水晒盐后,以其母液(卤水)和贝壳(主要成分是
)为原料制镁,其工艺流程如下图所示:

I、步骤①所加的碱应该是(选填"氢氧化钠"或"石灰乳"),步骤②反应的化学方程式是;若要验证镁、铁、铜的活动性顺序,选择铁丝后,还要选择、两种溶液。
II、
加热分解生成
和
,
是高熔点的化合物,某些阻燃剂(阻碍燃烧的物质)的有效成分是
。你认为
能够阻燃的原因可能是(选填序号)
| A. |
分解需要吸收大量的热,降低了可燃物的着火点 |
B. |
生成的氧化镁覆盖在可燃物表面,隔绝了空气 |
C. |
生成的水蒸气降低了可燃物周围氧气浓度 |
D. |
反应因吸热降低了环境温度,使可燃物不易达到着火点 |
铝、铜、铁是生活中常见的金属。
(1)铝在空气中具有很好的抗腐蚀性能的原因是
(2)用铜制电线主要是利用铜具有良好的性。
(3)铁制品锈蚀,实际上是铁跟空气中的发生了化学反应。焊接铁制品时,通常先用稀盐酸除去其表面的铁锈,反应的化学方程式为。防止铁制栏杆锈蚀的一种方法是。
人类目前所消耗的能量主要来自化石燃料。
(1)石油加热炼制得到的产品中,常用作汽车燃料的是(一种即可)。
(2)煤燃烧时排放出、等污染物,溶于雨水会形成酸雨。
(3)天燃气的主要成分是,它燃烧时将化学能主要转化为能。
用微粒的观点回答下列问题:
(1)保持水的化学性质的微粒是。
(2)水通电分解过程中,不变的微粒是。
(3)用湿抹布擦过的桌面,一段时间后变干的原因是。
(4)一定质量的水蒸气冷凝成水时,其体积变小的原因是。
下图是实验室常用的装置。请据图回答: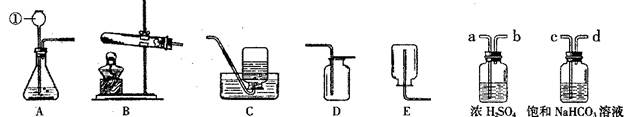
(1)写出仪器①的名称。收集某气体只能采用E装置,由此推测该气体具有的性质;
(2)用高锰酸钾制取氧气的装置组合是(填序号),反应的化学方程式为;
(3)实验室制得的
气体中常含有
和水蒸气。为了得到纯净、干燥的CO2气体,除杂装置的导管气流方向连接顺序是(填选项)。
| A. | a→b→c→d | B. | b→a→c→d |
| C. | c→d→a→b | D. | d→c→b→a |
向装有等量水的A、B、C烧杯中分别加入10g、25g、25gNaNO3固体,充分溶解后,现象如图一所示。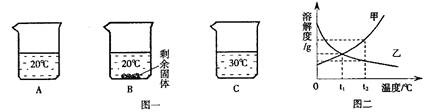
(1)烧杯中的溶液一定属于饱和溶液的是(填序号);
(2)图二能表示NaNO3溶解度曲线的是(填"甲"或"乙");
(3)由图二分析,若分别将100g甲、乙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述正确的(填序号)。
| A. |
甲、乙都是饱和溶液 |
B. |
所含溶剂质量:甲<乙 |
| C. |
溶液质量:甲>乙 |
D. |
溶质质量分数:甲>乙 |