科学家设想利用太阳能加热器"捕捉
"、"释放
",实现碳循环(如图所示)。

某化学小组的同学对此非常感兴趣,在老师的指导下,设计如下装置探究上述设想的反应原理是否可行。

(1)能证明装置
"释放
"的现象是;
(2)装置
在实验结束撤掉酒精喷灯时的作用是;
(3)上述反应结束后,小组同学对
中固体的成分进行探究,以证明是否"捕捉"到
。
【猜想与假设】
中的固体可能为:I.只有氧化钙;Ⅱ.氧化钙与碳酸钙;Ⅲ.只有碳酸钙
【进行实验】
①甲同学从
中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物。甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅲ成立。乙同学认为上述实验不足以证明猜想Ⅲ成立,其理由是。
②乙同学从
中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生。乙同学据此认为试管中的固体只有氧化钙,即猜想I成立。丙同学认为乙的实验不足以证明猜想I成立,理由是。
③丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和
稀盐酸证明了猜想Ⅱ成立,请完成他的实验报告。
| 实验步骤 |
实验现象 |
实验结论 |
|
|
|
猜想Ⅱ成立 |
(4)通过以上探究,小组同学认为科学家的设想在反应原理上是可行的。该设想的优点有(填字母序号)。
| A. |
原料易得 |
B. |
充分利用太阳能 |
C. |
释放出的 可作为资源加以利用 |
人类每年都要从大自然中提取大量的金属,用于满足日常生活和工农业生产的需要。
⑴某铁厂以焦炭、赤铁矿石(主要含Fe2O3)、空气等为原料炼铁,反应过程如下:
上述工艺流程中,步骤③发生反应的化学方程式为 ,
该反应中的还原剂是 。
⑵实验室常用下图装置模拟炼铁反应,实验开始时,须先通 CO,再用酒精喷灯加热,这样做的目的是 。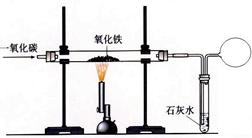
⑶我国古代即有湿法冶金技术,古书中就有“曾青得铁则化为铜”之说,请你写出铁能从硫酸铜溶液中置换出铜单质的原因: 。
⑷在众多的金属材料中,铝及其合金一直在人类生产、生活中占据着主导地位,工业上常采用电解氧化铝的方法来冶炼铝,该反应的化学方程式为 。
某兴趣小组利用下列装置进行实验室制取和收集气体的实验,请回答: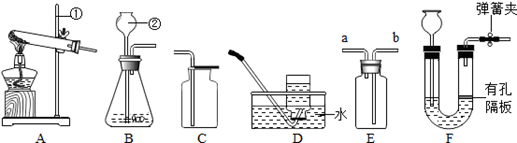
(1)指出仪器名称:②_______________。
(2)若用高锰酸钾制取纯净的氧气,应选用的制取装置是________(填字母),写出该反应的化学方程式_______________________________。若用C装置收集氧气,实验中始终未能检验到氧气已收满,下列解释不合理的是
| A.装置漏气 |
| B.药品用量可能不足 |
| C.导气管未伸到集气瓶底部 |
| D.药品可能失效 |
(3)实验室用装置B和F都可以制取氧气,若将发生装置由B改为F,其优点是 。
(4)若用E装置收集极易溶于水、密度比空气小的氨气,则气体应从______端进入(填“a”或“b”)
在“质量守恒定律”的教学中,老师引导同学们进行“化学反应中反应物与生成物的质量关系”的实验探究,请你参与探究并回答有关问题:
(1)如图A、B所示,将锥形瓶(反应物未接触)放在天平上,右盘加砝码使之平衡,取下锥形瓶,将锥形瓶中两种物质混合,反应完全后将锥形瓶再放回天平左盘上。
①A瓶重新放回到天平上,天平(填“能”或“不能”)保持平衡。
②B瓶重新放回到天平上,天平能否保持平衡?,理由是。
③从原子的角度分析“质量守恒定律” 。
(2)如上图C所示,用细线系住镁条使之平衡,然后在镁条一端用酒精灯加热。镁条在加热的条件下,能与空气中的氧气反应生成氧化镁。
①写出镁在空气中加热的文字表达式。
②加热一段时间后,镁条(填“能”或“不能”)保持平衡。
(3)某同学利用如图所示的装置测定空气中氧气的含量(体积分数)。他的操作过程如下(有100mL和500mL量筒供选用):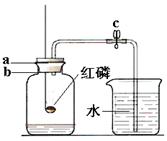
①检查整个装置的气密性后,将c处的止水夹夹紧,点燃红磷后,迅速插入左边的广口瓶中;
②待燃烧停止,整个装置冷却至室温后,将c处的止水夹打开。结果发现烧杯中的水进入到广口瓶中;
③待烧杯中的水不能再进入广口瓶后,打开广口瓶的橡胶塞,将广口瓶中的水全部倒入到100mL量筒中,测得其中水的体积为76ml。
④该同学又设法准确地测定了广口瓶中空气的体积,数据为400mL。
回答下列问题:①红磷燃烧时最明显的现象是___________________________;
②该同学测得的空气中氧气的体积分数为________%。与理论值21%相比较,产生误差的原因很可能是_____________________(导气管的体积可忽略不计)。
(6分)盐城是全国酸雨高发地区之一,某化学兴趣小组得知酸雨是因空气中的二氧化硫与水反应生成酸而导致,他们想对此进行探究,请你参与他们的探究过程:
(1)做出假设:;
(2)设计方案:用紫色的石蕊试液浸泡,制成紫色纸花并晾干。先验证水能否使紫色纸花变色,再验证二氧化硫气体能否使干燥的紫色纸花试纸变色,最后验证二氧化硫气体能否使湿润的紫色纸花变红,实验装置和药品如图:
(3)查阅资料:你认为该实验小组不需要掌握的资料内容中应包括(填序号);
①二氧化硫易溶于水②酸能使湿润的紫色石蕊试纸变红③SO2不与浓硫酸反应
(4)实验:①实验中纸花(Ⅱ)的颜色始终没有变化,这说明。
②纸花(Ⅲ)在实验过程中始终未见变色,此现象说明。
③实验Ⅰ的作用是。
(5)结论:实验过程中只有Ⅳ纸花变红,说明原假设(填“成立”或“不成立”)
某兴趣小组同学利用下图所示装置探究燃烧的条件。
【分析】(1)步骤①中白磷不燃烧的原因是。
(2)对比(填实验步骤的序号)可知燃烧需要氧气。
【结论】通过对实验分析,小组同学得出可燃物燃烧的条件是需要氧气、。
| 步骤 |
操作 |
现象 |
| ① |
打开K1,关闭K2 |
无明显现象 |
| ② |
打开K2,关闭K1 |
|
| ③ |
打开K2,关闭K1,将A中的液体滴入B中 |
C中有气泡冒出,白磷不燃烧 |
| ④ |
打开K1,关闭K2,将A中的液体滴入B中 |
D中有气泡冒出,白磷燃烧 |
【反思】(1)装置中的气球所起作用是。
(2)常言道“水火不相容”,但本实验步骤④中也观察到“水火相容”的奇观,其原因是。