合成氨反应为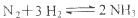 ,今有A、B、C、D四个容器,每个容器中有两种操作,两种操作分别达到平衡后,操作1中N2和操作2中NH3转化率之和一定不为1的是(起始体积相等)
,今有A、B、C、D四个容器,每个容器中有两种操作,两种操作分别达到平衡后,操作1中N2和操作2中NH3转化率之和一定不为1的是(起始体积相等)
A.恒温恒容:操作1:加1 mol N2+3 molH2,操作2:加2 mol NH3
B.恒温恒压:操作1:加1 mol N2+3 molH2,操作2:加2 mol NH3
C.恒温恒容:操作1:加1 mol N2+3 molH2,操作2:加3 mol NH3
D.恒温恒压:操作1:加1 mol N2+3 molH2,操作2:加3 mol NH3
对于反应2X(g)+Y(g)  2Z(g),下列说法正确的是()
2Z(g),下列说法正确的是()
| A.由于K=c2(Z)/[c2(X)·c(Y)],随着反应的进行,Z的浓度不断增大,X,Y的浓度不断减小,平衡常数不断增大 |
| B.当温度不变时,增大反应物的浓度,使K变小;增大生成物的浓度,使K增大 |
| C.可逆反应达到平衡时,逆反应便立即停止了 |
| D.温度发生变化,上述的K值也发生变化 |
温度一定时,用水稀释0.1 mol·L-1氨水时,随着水量的增加而减小的是()
| A.c(OH—)·c(NH4+)/c(NH3·H2O) | B.c(NH3·H2O)/c(OH—) |
| C.c(H+)和c(OH_)的乘积 | D.OH—的物质的量 |
在给定条件的水溶液中一定能大量共存的离子组是()
| A.能与Al反应生成H2的溶液:Ca2+、NH4+、HCO3-、Cl- |
| B.c(Fe2+)=0.05mol/L的溶液:H+、Na+、NO3-、SO42- |
| C.常温下,pH=12的溶液:Na+、K+、Cl-、NO3- |
| D.常温下,由水电离的c(H+)=10-12mol/L的溶液:K+、Ba2+、ClO-、NO3- |
下列离子方程式表达正确的是( )
| A.等体积,等物质的量浓度的NaHCO3溶液和Ca(OH)2溶液混合:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| B.FeI2溶液中通入少量氯气:2Fe2++Cl2= 2Fe3++2Cl- |
C.CH3COONH4的电离:CH3COONH4 NH4++CH3COO- NH4++CH3COO- |
| D.用食醋除去水瓶中的水垢:CO32-+2CH3COOH==2CH3COO-+CO2↑+H2O |
NA代表阿伏加德罗常数,下列叙述错误的是()
| A.在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移2NA个电子 |
| B.1 mol羟基中电子数为10NA |
| C.标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g |
| D.常温下,1 L 0.1 mol·L-1的NH4NO3溶液中氮原子数为0.2NA |