用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A.62gNa2O溶于水后所得溶液中含有的O2-数为NA |
| B.标准状况下,NA个三氧化硫分子所占据的体积约是22.4L |
| C.常温常压下,16g甲基(—13CH3)所含的中子数为7NA |
D.10L0.1mol·L-1的Na2CO3溶液中,Na+、CO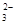 总数为3NA 总数为3NA |
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH3CH2OH – 4e- + H2O = CH3COOH + 4H+。下列有关说法正确的是()
| A.检测时,电解质溶液中的H+向负极移动 |
| B.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气 |
| C.电池反应的化学方程式为:CH3CH2OH + O2 = CH3COOH + H2O |
| D.正极上发生的反应为:O2 + 4e- + 2H2O = 4OH- |
水溶液X中只可能溶有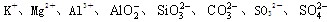 中的若干种离子。某同学对该溶有进行了如下实验:
中的若干种离子。某同学对该溶有进行了如下实验: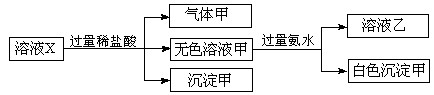
下列判断正确的是()
| A.气体甲一定是纯净物 |
| B.沉淀甲是硅酸和硅酸镁的混合物 |
C.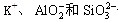 一定存在于溶液X中 一定存在于溶液X中 |
D.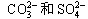 一定不存在于溶液X中 一定不存在于溶液X中 |
科学家最近研制出可望成为高效火箭推进剂的N(NO2)3(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法正确的是( ) 
| A.分子中N、O间形成的共价键是非极性键 |
| B.分子中四个氮原子共平面 |
| C.该物质既有氧化性又有还原性 |
| D.15.2 g该物质含有6.02×1022个原子 |
下列离子方程式正确的是()
| A.钠与水反应:Na + 2H2O = Na+ + 2OH- + H2↑ |
| B.硅酸钠溶液与醋酸溶液混合:SiO32- + 2H+ = H2SiO3↓ |
| C.0.01mol/LNH4Al(SO4)2溶液与0.02mol/LBa(OH)2溶液等体积混合: NH4+ +Al3+ + 2SO42- + 2Ba2+ + 4OH- = 2BaSO4↓ + Al(OH)3↓ + NH3·H2O |
D.浓硝酸中加入过量铁粉并加热:Fe + 3NO3- + 6H+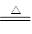 Fe3+ + 3NO2↑ + 3H2O Fe3+ + 3NO2↑ + 3H2O |
下列离子组一定能大量共存的是()
| A.甲基橙呈黄色的溶液中:I-、Cl-、NO3-、Na+ |
| B.石蕊呈蓝色的溶液中:Na+、AlO2-、NO3-、HCO3- |
| C.含大量Al3+的溶液中:K+、Na+、NO3-、ClO- |
| D.含大量OH一的溶液中:CO32-、Cl-、F-、K+ |