高压下氮气聚合生成高聚氮,其晶体中每个氮原子都通过三个单键与其他氮原子结合并向空间发展构成立体网状结构。已知晶体中N—N键的键能为160 KJ/mol,而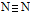 的键能为942 KJ/mol。则下列说法不正确的是
的键能为942 KJ/mol。则下列说法不正确的是
| A.键能越大说明化学键越牢固,所构成的物质越稳定 |
| B.高聚氮晶体属于原子晶体 |
| C.该晶体中氮原子数与氮氮键数比为1:3 |
| D.高聚氮可以用作炸药 |
实验中的下列操作正确的是
| A.取出试剂瓶中的Na2CO3溶液,加入试管中,发现取量过多,为了不浪费,又把试管中过量的试剂倒回原试剂瓶中 |
| B.Ba(NO3)2 溶于水,可将含有Ba(NO3)2 的废液倒入水池中,再用水冲入下水道 |
| C.用蒸发方法使NaCl 从溶液中析出时,应将蒸发皿中NaCl 溶液全部蒸干才停止加热 |
| D.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 |
下图为反应Fe + CuSO4=Cu + FeSO4中电子转移的关系图,则图中的元素甲、乙分别表示
| A.Fe,S |
| B.Cu,S |
| C.Fe,O |
| D.Fe,Cu |
下列基本反应类型中,一定是氧化还原反应的是
| A.置换反应 | B.分解反应 | C.化合反应 | D.复分解反应 |
下列操作过程中一定有氧化还原反应发生的是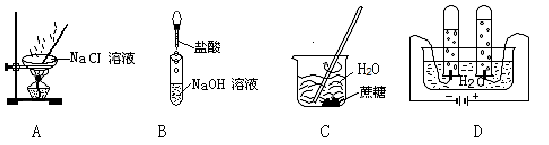
有关氧化还原反应实质的说法中正确的是
| A.是否有元素的电子转移 | B.是否有元素的化合价的变化 |
| C.是否有氧元素的参加 | D.是否有原子的重新组合 |