某学生用浓度为0.1 mol/L左右的KOH溶液滴定未知浓度的盐酸,有如下操作步骤:
(A)移取20.00 mL待测的盐酸注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用KOH溶液润洗滴定管2—3次
(C)把盛有KOH溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取KOH溶液注入碱式滴定管至0刻度以上2—3 cm
(E)调节液面至O或0刻度以下,记下读数
(F)把锥形瓶放在滴定管的下面,用KOH溶液滴定至终点,记下滴定管液面的刻度
回答下列问题:
(1)正确操作的顺序是 (填编号)
(2)实验室可提供下列浓度的KOH浓液,应选用的是 。(填编号)
A.0.1 mol/L B.O.10 m01/L C.O.1032 mol/L
(3)(A)操作中量取待测液的仪器是 o
(4)(B)操作的目的是 .
(5)(F)操作中判断到达终点的现象是 。
(6)(B)如被省略所测结果 (填“偏大”、“偏小”、“不变”).
(7)KOH溶液在空气中易变质生成 ,该物质水溶液PH 7,其水溶液中离子浓度大小排序为
(8)(C)步如何使滴定管尖嘴充满溶液
在密闭容器中,丁烷催化裂解,其碳链按两种方式断裂,生成两种烷烃和两种烯烃。若
丁烷的裂解率为90%,求裂解后混合气体的平均相对分子质量__________。
金刚烷(可以看成四个等同的六元环组成的空间构型)是一种重要的化工原料,工业上
可通过下列途径制备: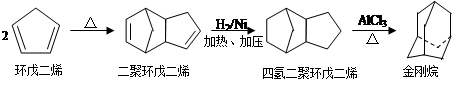
请回答下列问题:
(1)环戊二烯分子中最多有____________个原子共平面;
(2)金刚烷的分子式为_______________,其分子中的—CH2—基团有_____________个;金刚烷的二
氯代物的数目是______。
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:
其中,反应①的产物名称是_________________,反应②的反应试剂和反应条件_____________,反
应③的反应类型是___________;
【化学——选修有机化学基础】
下图中 A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物。
根据上图回答问题:
(1)已知E的相对分子质量为102,其中碳、氢两种元素的质量分数分别为58.8%、9.8%,其余为氧,则E的分子式为。
(2)化合物B不能发生的反应是(填字母序号):
a.加成反应 b.取代反应 c.消去反应 d.酯化反应 e.水解反应 f.置换反应
(3)反应②的化学方程式是。
(4)C分子中的官能团名称是;A的结构简式是。
(5)同时符合下列三个条件的B的同分异构体的数目有个。
Ⅰ.含有间二取代苯环结构 Ⅱ.属于非芳香酸酯 Ⅲ.与 FeCl3溶液发生显色反应。写出其中任意一个同分异构体的结构简式。
【化学-物质结构与性质】
N和B元素在化学中有很重要的地位。
(1)写出与N元素同主族的As元素的基态原子核外电子排布式_________________。
从原子结构的角度分析B、N和O元素的第一电离能由大到小的顺序为___________。
(2)N元素与B元素的氟化物化学式相似,均为AB3型,但分子的空间结构有很大不同,其原因是_____________________________________________,其中BF3的分子构型为__________。
(3)立方氮化硼可利用人工方法在高温高压条件下合成,其硬度仅次于金刚石而远远高于其它材料,因此它与金刚石统称为超硬材料。BN的晶体结构与金刚石相似,其中B原子的杂化方式为________,微粒间存在的作用力是________。
(4)NaN3是抗禽流感药物“达菲”合成过程中的中间活性物质,NaN 3也可用于汽车的保护气囊。3 mol NaN 3受撞击会生成4 mol N2气体和一种离子化合物A。
①请写出上述NaN 3撞击反应的化学方程式。
②根据电子云的重叠方式判断:N2分子中存在的σ键和π键数目之比为。
)【化学—选修化学与技术】
工业上以磷肥生产形成的副产物石膏(CaSO4·2H2O)与焦炭为原料可生产硫酸,同时
可以得到硫酸钾肥料和氯化钙水合物储热材料。以下是有关的工艺流程示意图。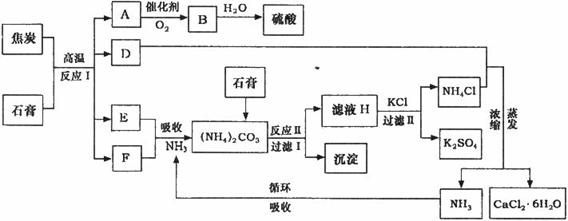
试回答:
(1)写出方程式:反应Ⅰ___________________________________,
(2)写出方程式:反应Ⅱ______________________________________。
(3)请根据下表和化学平衡知识,分析工业上制硫酸中SO2的催化氧化的适宜条件是
____________________________________。
表Ⅰ:
 压强 / M Pa 压强 / M Pa转化率/% 温度/℃ |
0.1 |
0.5 |
1 |
10 |
| 400 |
99.2 |
99.6 |
99.7 |
99.9 |
| 500 |
93.5 |
96.9 |
97.8 |
99.3 |
| 600 |
73.7 |
85.8 |
89.5 |
96.4 |
(4)检验滤液H中含有CO 的方法是___________________________________。
的方法是___________________________________。
(5)氯化钙结晶水合物( )是目前常用的无机储热材料,选择的依据是___________ (填序号)。
)是目前常用的无机储热材料,选择的依据是___________ (填序号)。
a.熔点较低(29℃熔化) b.能导电 c.易溶于水 d.无毒