已知:H2(g)+F2(g)===2HF(g) ΔH=-270 kJ/mol,下列说法正确的是( )
| A.2 L氟化氢气体分解成1 L氢气与1 L氟气吸收270 kJ热量 |
| B.1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ |
| C.在相同条件下,1 mol氢气与1 mol氟气的能量总和大于2 mol氟化氢气体的能量 |
| D.1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270 kJ热量 |
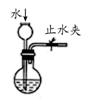
下列装置或操作能达到实验目的的是( )
 |
 |
 |
 |
| A.实验室制取并收集NH3 |
B.用乙醇提取溴水中的溴 |
C.检查装置气密性 |
D.利用排空气法收集CO2 |
广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其他简单仪器组成各种功能的装置。下列各图中能用作防倒吸安全瓶的是( )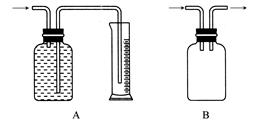

下列实验问题的处理方法中,正确的是( )
| A.实验中不慎打破温度计,可用吹风机吹风加快水银(Hg)的挥发 |
| B.在气体发生装置上直接点燃甲烷(CH4)气体时,必须先检验甲烷的纯度 |
| C.实验结束后,将废液倒入下水道排出实验室,以免污染实验室 |
| D.制取NH3实验中,将多余NH3用导管直接导入水槽,用水吸收 |
下列试剂保存方法不正确的是( )
| A.AgNO3存放在棕色瓶中 |
| B.用铝制容器装运浓硝酸 |
| C.少量白磷保存在水中 |
| D.溴水存放在带橡胶塞的玻璃瓶中 |
对于易燃、易爆、有毒的化学物质,往往会在其包装上贴以下危险警告标签。下面所列物质中,贴错了标签的是( )
| A |
B |
C |
D |
|
| 物质的 化学式 |
HNO3(浓) |
CCl4 |
KCN |
KClO3 |
| 危险警告标签 |
 腐蚀品 |
 易燃品 |
 剧毒品 剧毒品 |
 爆炸品 爆炸品 |