(14分)下表为元素周期表的一部分:(用元素符号或化学式填空)
| 族 周期 |
|
|
|
|||||
| |
① |
|
|
|
|
|
|
|
| |
|
|
|
|
|
② |
|
|
| |
③ |
|
|
④ |
|
⑤ |
⑥ |
|
(1)写出元素④在周期表中的位置______________。
(2)②、③、⑤的原子半径由大到小的顺序为_________________________。
(3)④、⑤、⑥的气态氢化物的稳定性由强到弱的顺序是_________________________。
(4)①、②、③、⑥中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
Ⅱ.由上述部分元素组成的物质间,在一定条件下,可以发生下图所示的变化,其中A是一种淡黄色固体。请回答:
(1)写出固体A与液体X反应的离子方程式 。
(2)气体Y是一种大气污染物,直接排放会形成酸雨。可用溶液B吸收,当B与Y物质的量之比为1:1且恰好完全反应时,所得溶液D的溶质为 (填化学式)。
(3)写出气体C与气体Y反应的化学方程式 。
某同学做元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验步骤”与“实验现象”前后不一定是对应关系)。
| 实验步骤 |
实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 |
A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色。 |
| ②向新制得的Na2S溶液中满加新制的氯水 |
B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 |
C.剧烈反应,迅速产生大量无色气体. |
| ④将镁条投入稀盐酸中 |
D.反应不十分剧烈;产生无色气体。 |
| ⑤将铝条投入稀盐酸中 |
E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 |
F.生成淡黄色沉锭。 |
请你帮助该同学整理并完成实验报告。
(1)实验内容:(填写与实验步骤对应的实验现象的编号和②③的化学方程式)
| 实验内容 |
① |
② |
③ |
④ |
⑤ |
⑥ |
| 实验现象(填A~F) |
实验② ,
实验③ ;
(2)实验结论: 。
将20g Ba(OH)2·8H2O晶体与10 g NH4Cl晶体一起放入小烧杯中,将烧杯放在滴有3~4滴水的玻璃片上,用玻璃棒迅速搅拌。
(1)实验中玻璃棒的作用是。
(2)写出有关反应的化学方程式。
(3)实验中观察到的现象有、和反应混合物成糊状。
(4)通过现象,说明该反应为(填“吸热”或“放热”)反应,这是由于反应物的总能量(填“小于”或“大于”)生成物的总能量。
某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol· L-1盐酸、0.55mol· L-1NaOH溶液,尚缺少的实验玻璃用品是、。
(2)他们记录的实验数据如下:
| 实验用品 |
溶液温度 |
中和热△H |
|||
| t1 |
t2 |
||||
| ① |
50mL0.55mol.L-1NaOH |
50mL.0.5mol.L-1HCl |
20℃ |
23.3℃ |
|
| ② |
50mL0.55mol.L-1NaOH |
50mL.0.5mol.L-1HCl |
20℃ |
23.5℃ |
已知:Q=Cm(t2 -t1),反应后溶液的比热容C为4.18KJ·℃-1· Kg-1,各物质的密度均为1g·cm-3。
计算完成上表。△H=
(3)某研究小组将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50 mL)。回答下列问题:
研究小组做该实验时环境温度(填“高于”、“低于”或“等于”)22 ℃,此反应所用NaOH溶液的浓度应为mol/L。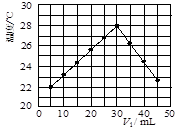
除去下列物质中所含的杂质,将除杂质试剂和操作方法填入空格。
| 物质 |
杂质 |
除杂试剂 |
操作方法 |
|
| 1) |
苯 |
苯酚 |
||
| 2) |
乙炔 |
硫化氢 |
||
| 3) |
溴苯 |
溴 |
||
| 4) |
柴油 |
汽油 |
_____________ |
实验室制取乙烯的装置如右图所示,请根据图示回答下列问题: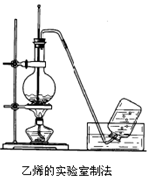
(1)该反应类型属于_________________________;
实验室制乙烯的化学方程式为_________________________________________________
(2)某化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启
发他们并由他们自己设计了下列实验图以确认上述混合气体中有C2H4和SO2。回答下列
问题: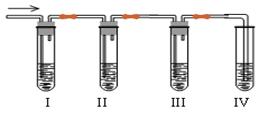
①、I、II、Ⅲ、IV装置可盛放的试剂是IIIⅢIV____(填试剂的序号)。
| A.品红溶液 | B.NaOH溶液 | C.浓硫酸 | D.酸性KMnO4溶液 |
②、能说明SO2气体存在的现象是_____________________________________________。
③、使用装置II的目的是_____________________________________________________。
④、使用装置Ⅲ的目的是_____________________________________________________。
⑤、确定含有乙烯的现象是____________________________________________________