苯甲酸广泛应用于制药和化工行业。某同学尝试用甲苯的氧化反应制备苯甲酸。反应原理:
实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。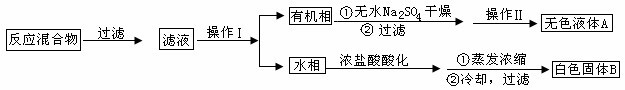
已知:苯甲酸相对分子质量是122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3g和6.9g;纯净固体有机物一般都有固定熔点。
(1)操作Ⅰ为 ,操作Ⅱ为 。
(2)无色液体A是 ,定性检验A的试剂是 ,现象是 。
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔。该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请在答题卡上完成表中内容。
| 序号 |
实验方案 |
实验现象 |
结论 |
| ① |
将白色固体B加入水中,加热,溶解,Ⅰ |
得到白色晶体和无色溶液 |
———— |
| ② |
取少量滤液于试管中, Ⅱ |
生成白色沉淀 |
滤液含有Cl- |
| ③ |
干燥白色晶体, Ⅲ |
Ⅳ |
白色晶体是苯甲酸 |
(4)纯度测定:称取1.220g产品,配成100ml甲醇溶液,移取25.00ml溶液,滴定,消耗KOH的物质的量为2.40×10-3mol。产品中苯甲酸质量分数为 (保留两位有效数字)。
(10分)为测定某碳酸氢钠样品纯度(含有少量氯化钠),学生设计了如下几个实验方案(每个方案均称取m1g样品),请回答每个方案中的问题。
[方案Ⅰ] 选用重量法进行测定:可用下图中的装置进行实验。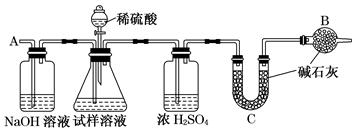
(1)A装置中NaOH溶液的作用是__________________若直接向试样溶液中鼓入空气会导致实验测定结果________(填“偏高”、“偏低”或“无影响”)。
(2)该方案需直接测定的物理量是______________________________________。
[方案Ⅱ] 选用气体体积法进行测定:可用如图中的装置进行实验,为了减小实验误差,量气管中加入饱和NaHCO3溶液。
(3)通过实验,测得该试样中碳酸氢钠质量分数偏低,产生这种现象
的原因可能是________。
a.测定气体体积时未冷却至室温
b.测定气体体积时水准管的液面高于量气管的液面
c.Y型管中留有反应生成的气体
d.气体进入量气管前未用浓硫酸干燥
[方案Ⅲ] 选用滴定法进行测定:
(4)称取m1g样品,配成100 mL溶液,取出20 mL,用c mol·L-1的标准HCl溶液滴定,
消耗体积为VmL,则该试样中碳酸氢钠质量分数的计算表达式为:_________________
实验室里通常用MnO2与浓盐酸反应制取氯气。现用下列有关装置先制取干燥、纯净的氯气。后进行有关性质实验。试根据下列有关装置回答有关问题。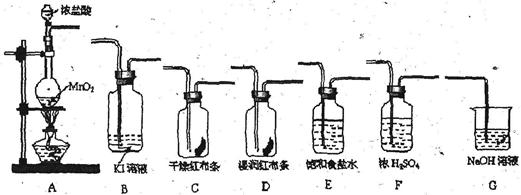
(1)上述装置中各仪器从左至右的连接顺序为A接__接__接__接__接__接G。
(2)E装置的作用是__________,D中的现象为____,B中的现象为_________。
(3)写出相关反应的离子方程式:A中___________,G中______________。
(4)某温度下,将Cl2通入NaOH溶液中,反应得到含有ClO-与ClO3-物质的量之比为1:1的混合液,反应的化学方程式是______________________________________。
(5) 报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是(用离子方程式表示)_______________________________________。
(19分)实验室欲用胆矾配制250 mL0.2 mol·L-1的CuSO4溶液。
(1)配制溶液时,一般可以分为以下几个步骤:(完成下列空格)
A 计算B 称量 C.溶解D.______E. ______F. 定容 G. 摇匀、装瓶
(2)本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、量筒还有______
和______(填仪器名称)
(3)经计算需要称取CuSO4·5H2O的质量为______。
(4)若称取胆矾时砝码被放在左盘(10g以下用游码),则配制的CuSO4溶液的浓度______(填“偏高”、“偏低”、“无影响”);若定容时仰视刻度线,则配制的CuSO4溶液的浓度______ (填“偏高”、“偏低”、“无影响”)。
(5)从准确配制好的CuSO4溶液中取出50mL ,则这50mL CuSO4溶液的物质的量浓度为______________,所含Cu2+的质量为。
下图所示是分离混合物时常用的仪器,回答下列问题: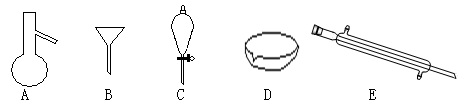
(1)写出仪器C、E的名称、
(2)分离以下混合物应该主要选用上述什么仪器?(填字母符号)
①NaCl固体和泥沙:②花生油和水:
(3)若向C装置中加入碘水和足量CCl4,充分振荡后静置,观察到现象是:C内液体分两层,上层液体呈色,下层液体色。
(4)碘单质和溴单质有相类似的性质,都可以用有机溶剂萃取水溶液中的单质,若利用C仪器提取溴水中的溴单质,下列有机溶剂中不能选用的是:
A.汽油 B.CCl4C.酒精 D.醋酸
已知25℃、101 kPa下,稀的强酸与强碱溶液反应的中和热为57.3 kJ/mol。
(1)写出表示稀硫酸与稀烧碱溶液发生反应的中和热的热化学方程式:。
(2)学生甲用稀硫酸与稀烧碱溶液测定中和热装置如图。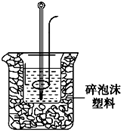
①实验时所需的玻璃仪器除烧杯、量筒外还需:。
②该装置中有一处错误是:,如果用该错误装置测定,结果会(填“偏
高”“偏低”“无影响”)
③如果,该生用50 mL 0.25 mol/L的稀硫酸与50 mL 0.55 mol/L的稀烧碱溶液,他用试剂的用量的理
由是:。在该实验中需要测定某种数据,
完成一次实验,需要测定该数据的次数为次。
(3)学生乙用2 mol/L的硫酸来测定与锌粒和锌粉反应的快慢,设计如图(Ⅰ)装置:

图Ⅰ图Ⅱ
①该生两次实验测定时间均设定为10 min,那么他还要测定的另一个数据是:
。
②如果将图Ⅰ装置中的气体收集装置改为图Ⅱ,实验完毕待冷却后,该生准备读取滴定管上液面所处的刻度数,发现滴定管中液面高于干燥管中液面,应先采取的操作是:。③该实验结果中,你估计与酸反应较快的是。