活性氧化锌是一种多功能性的新型无机材料,其颗粒大小约在1-100纳米。某化工冶金研究所采用湿化学法(NPP-法)制备纳米级活性氧化锌,可用各种含锌物料为原料,采用酸浸出锌,经过多次净化除去原料中的杂质,然后沉淀获得碱式碳酸锌,最后焙解获得活性氧化锌,化学工艺流程如下: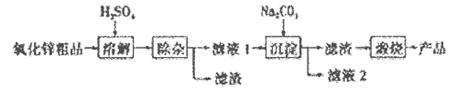
(1)通过__________(填操作名称)可以检验流程中滤液2中含有Na+。
(2)若上述流程图中Na2CO3溶液的pH=12,下列说法正确的是___________。
A该溶液中
B.该溶液中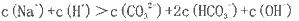
C.该溶液中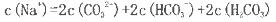
D.若将该溶液稀释至100倍,则pH=10。
(3)“溶解”后得到的酸性溶液中含有Zn2+、SO42-,另含有Fe2+、Cu2+等杂质。取0.5L该溶液先加入___________(填“Na2CO3”或“H2SO4”)调节溶液的pH至5.4,然后加入适量KMnO4,Fe2+转化为Fe(OH)3,同时KMnO4转化为MnO2。经检测溶液中Fe2+的浓度为0 009 mol/L,则该溶液中至少应加入_______molKMnO4 .
某化学研究性学习小组的同学在学习了电化学相关知识后,将所学知识整合得到如图所示装置,用于电解饱和食盐水。
请回答下列问题:
(1)甲池中Al极为 极,乙池中C2极为 极;
(2)甲池中发生反应的总化学方程式为 ;
(3)若向乙池中滴加酚酞试液,则C1极附近观察到的现象为 ,C2极的电极反应式为 ;
(4)当C1极析出224mL气体(标准状况)时,转移电子的物质的量为 。
(14分)丙烯酸乙酯(Ⅳ)是合成塑料、树脂等高聚物的重要中间体,可由下面路线合成:
(1)反应②属于 反应,1molⅣ完全燃烧消耗O2为 mol.
(2)Ⅱ含有的官能团名称为 ,Ⅱ能使溴水褪色,其反应方程式为 .
(3)Ⅰ可以由Ⅴ(分子式为C3H6O)催化氧化得到,则Ⅴ→Ⅰ的反应方程式为 (注明反应条件).
(4)Ⅵ是Ⅳ的一种无支链的同分异构体,且碳链两端呈对称结构.则Ⅵ的结构简式为 .
(5)一定条件下,化合物  也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为 .
也可与化合物Ⅲ发生类似反应③的反应,则得到的产物的结构简式为 .
(6分)一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示: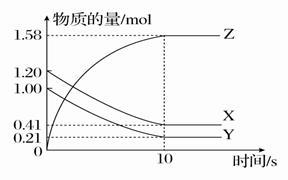
(1)从反应开始到10 s,用Z表示的反应速率为________。X的物质的量浓度减少了___________,Y的转化率为________。
(2)该反应的化学方程式为_____________________。
(3)10 s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图象如图所示: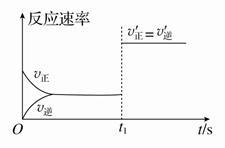
则下列说法符合该图像的是________。
| A.t1时刻,增大了X的浓度 | B.t1时刻,升高了体系温度 |
| C.t1时刻,缩小了容器体积 | D.t1时刻,使用了催化剂 |
(5分)麻醉剂的发现和使用,是人类医疗史上了不起的一项成就,它可使患者在接受治疗中感觉不到疼痛。
(1)一种常用的麻醉剂氯仿(CHCl3),常因保存不善被氧化而变质,产生剧毒物光气(COCl2)。
2CHCl3+O2 2HCl+2COCl2.为防止发生事故,使用前可用于检验是否变质的试剂是(填序号)________。
2HCl+2COCl2.为防止发生事故,使用前可用于检验是否变质的试剂是(填序号)________。
| A.淀粉碘化钾溶液 | B.NaOH溶液 |
| C.酚酞溶液 | D.硝酸酸化的硝酸银溶液 |
(2)稀有气体氙气(Xe)在医疗上很受重视,常常作为麻醉剂,氙气能溶于细胞的油脂里,引起细胞麻醉和膨胀,从而神经末梢作用暂时停止。人们曾试用体积分数为80%氙气和20%的氧气组成的混合气体,作为无副作用的麻醉剂。氙在元素周期表中位于_______周期,______族,它的原子序数是______。
(3)作为稀有气体,氙的化学性质不活泼,但它可在一定条件下生成化合物。取1molXe和3.5mol氟气于一密闭容器内充分反应,后来余下了1.5mol的氟气同时有白色固体生成,此白色固体的化学式为_________。
(7分)有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有全部标出)。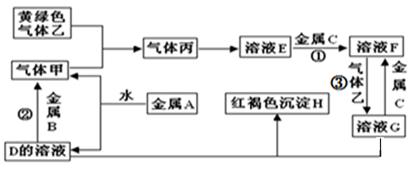
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A__________;H ___________; G__________;乙_________;
(2)写出下列反应的化学方程式
反应①________________
反应②________________
反应③_________________