如图 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路后发现
为电镀槽.接通电路后发现 上的c点显红色.为实现铁上镀锌,接通
上的c点显红色.为实现铁上镀锌,接通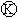 后,使c、d两点短路.下列叙述正确的是
后,使c、d两点短路.下列叙述正确的是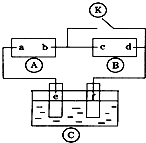
| A.a为直流电源的负极 | B.c极发生的反应为2H++2e-=H2↑ |
| C.f电极为锌板 | D.e极发生还原反应 |
对于反应aX(g)+bY(g) cZ(g)+dR(g) △H=QkJ/mol反应开始时,容器内充入X、Y或Z、R如图所示表示反应达到平衡后,图1、图2分别表示反应达到平衡后,改变温度和压强对反应的影响,下列叙述中正确的是
cZ(g)+dR(g) △H=QkJ/mol反应开始时,容器内充入X、Y或Z、R如图所示表示反应达到平衡后,图1、图2分别表示反应达到平衡后,改变温度和压强对反应的影响,下列叙述中正确的是
| A.开始时充入X和Y a+b>c+d Q<0 |
| B.开始时充入X和Y a+b>c+d Q>0 |
| C.开始时充入Z和R a+b>c+d Q<0 |
| D.开始时充入Z和R a+b<c+d Q>0 |
反应3Fe(s)+4H2O(g)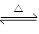 Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
| A.把Fe粉变成Fe片 |
| B.将容器的体积缩小一半 |
| C.保持容积不变,充入N2使容器压强增大 |
| D.压强不变,充入N2使容器体积增大 |
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如右图所示,下列描述正确的是: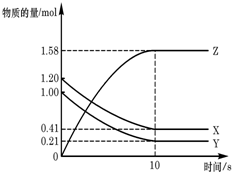
| A.反应开始到10s,用Z表示的反应速率为0.158mol/(L•s) |
| B.反应开始到10s,X的物质的量浓度减少了0.79mol/L |
| C.反应开始到10s时,Y的转化率为79.0% |
D.反应的化学方程式为:X(g)+Y(g) Z(g) Z(g) |
已知某条件下,合成氨反应的数据如下:N2(g)+3H2(g) 2ΝΗ3(g)
2ΝΗ3(g)
| 起始浓度/mol•L-1 |
1.0 |
3.0 |
0.2 |
| 2s末浓度/mol•L-1 |
0.6 |
1.8 |
1.0 |
| 4s末浓度/mol•L-1 |
0.4 |
1.2 |
1.4 |
当用氨气浓度的增加来表示该反应的速率时,下列说法中错误的是
A.2s末氨气的反应速率=0.4mol•(L•s)-1
B.前2s时间内氨气的平均反应速率=0.4mol•(L•s)-1
C.前4s时间内氨气的平均反应速率=0.3mol•(L•s)-1
D.2~4s时间内氨气的平均反应速率=0.2mol•(L•s)-1