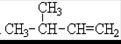某同学发现,纯度、质量、表面积都相同的两铝片与c(H+)相同的盐酸和硫酸在同温同压下反应时产生氢气的速率差别很大,铝与盐酸反应速率更快。他决定对其原因进行探究。填写下列空白:
(1)该同学认为:由于预先控制了反应的其他条件,那么,两次实验时反应的速率不一样的原因,只有以下五种可能:原因Ⅰ:Cl-对反应具有促进作用,而SO42-对反应没 有影响;
原因Ⅱ:_________________________________;
原因Ⅲ:Cl-对反应具有促进作用,而SO42-对反应具有阻 碍作用;
原因Ⅳ:Cl-、SO42-都对反应具有促进作用,但Cl-影响更大;
原因Ⅴ: _________________________________。
(2)该同学设计进行了两组实验,即得出了正确的结论。他取了两片等质量、外形和组成相同、表面经过砂纸充分打磨的铝片,分别放入到盛有同体积、c(H+)相同的稀硫酸和盐酸的试管(两试管的规格相同)中:
①在盛有硫酸的试管中加入少量NaCl或KCl固体,观察反应速率是否变化。
②在盛有盐酸的试管中加入少量Na2SO4或K2SO4固体,观察反应速率是否变化。
③若观察到实验①中_____ ,实验②中_____ ,则说明原因Ⅲ是正确的。依此类推。该同学通过分析实验现象,得出了结论:Cl-对反应具有促进作用。
.某烃A的相对分子质量为84。回答下列问题:
(1)下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是(填序号)________。
a.C7H12O2 b.C6H14c.C6H14O d.C7H14O3
(2)若烃A为链烃,与HBr加成后只能得到一种产物,且该烃的一氯代物只有一种。
①A的结构简式为________________;
②链烃A与Br2的CCl4溶液反应生成B,B与NaOH的醇溶液共热可得到D,D分子中无溴原子。请写出由B制备D的化学方程式:__________________;
③B与足量NaOH水溶液完全反应,生成有机物E,该反应的化学方程式:_______________________________;E与乙二醇的关系是_______________。
(3)若核磁共振氢谱显示链烃A有三组不同的峰,峰面积比为3:2:1,则A的名称为__________________。
(4)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为
按要求填空:
(1)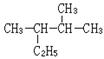 的系统命名为
的系统命名为
(2)松油醇(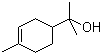 )的分子式为
)的分子式为
(3)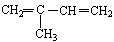 与Br2以物质的量之比为1:1反应,所得产物有种(不考虑顺反异构)
与Br2以物质的量之比为1:1反应,所得产物有种(不考虑顺反异构)
(4) 与新制的氢氧化铜在加热条件下反应的化学方程式
与新制的氢氧化铜在加热条件下反应的化学方程式
某有机物A,由C、H、O三种元素组成,在一定条件下,由A可以转化为有机物B、C和D、E;C又可以转化为B、A。它们的转化关系如下: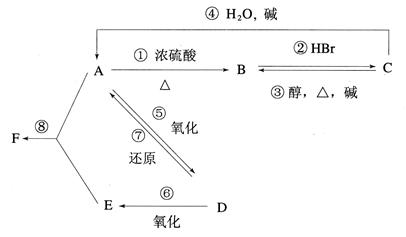
已知D的蒸气密度是氢气的22倍,并可以发生银镜反应。
⑴A~F的结构简式依次为____________、____________、____________、____________、____________、____________。
⑵在①~⑧的转化中属于消去反应的有____________加成反应的有____________取代反应的有____________。
⑶(在A~F中,选择适当的字母填空)适用于制作食品包装袋的单体是__________。常温下能与新制Cu(OH)2反应的是_______________,目前提倡用于和汽油按一定比例混合作汽车发动机燃料的是________________。
(4)分别写出①⑤的化学方程式。
请根据官能团的不同对下列有机物进行分类。(将序号填入空格处)(共8分)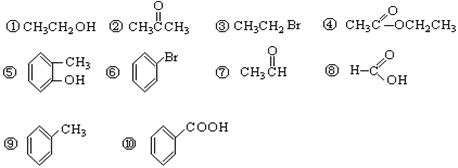
(1)芳香烃:;(2)卤代烃:;(3)醇:
(4)酚:;(5)醛:;(6)酮:
(7)羧酸:;(8)酯:。
用系统命名法命名下列物质(共6分)
①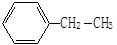 ②
② 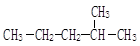 ③
③