下列说法正确的是
| A.两种原子形成的共价键一定是极性共价键 |
| B.元素金属性越强,对应单质的还原性越强;元素非金属性越强,对应单质的氧化性越强 |
| C.由金属元素和非金属元素组成的化合物一定是离子化合物 |
| D.按照元素周期表的排布规律,非金属元素最多有23种 |
现有短周期主族元素X、Y、Z、R、T。R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T化合物能破坏水的电离平衡。六种元素的原子半径与原子序数的关系如图所示。下列推断正确的是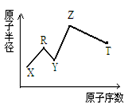
| A.原子半径和离子半径均满足:Y<Z |
| B.氢化物的沸点排序:Y>T>R |
| C.最高价氧化物对应的水化物的酸性:T<R |
| D.由X、R、Y、Z四种元素组成的化合物水溶液一定显碱性 |
下列说法错误的是
| A.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
| B.能自发进行的化学反应,焓变和熵变一定符合:△H<0、△S>0 |
| C.将碳酸钠溶液和碳酸氢钠溶液分别蒸干并灼烧,所得固体的成分均为纯碱 |
| D.用FeCl3饱和溶液制Fe(OH)3胶体的过程属于吸热过程 |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.使苯酚显紫色的溶液:NH4+ 、K+、SCN-、SO42- |
| B.使甲基橙变红色的溶液:Mg2+、K+、SO42-、NO3- |
| C.由水电离的c(OH-)=10-13mol·L-1的溶液中:Na+、Cl-、CO32-、NO3- |
| D.c(Fe2+)=1.0 mol·L-1溶液:H+、K+、Cl-、NO3- |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.常温常压下,4.4 g CO2与N2O混合气体中含有的原子总数为0.3NA |
| B.标准状况下,2.24L己烷含有分子的数目为0.1NA |
| C.1 L 1 mol·L-1的CuCl2溶液中含有Cu2+的数目为NA |
| D.在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
经一定时间后,可逆反应aA+bB  cC中物质的含量A%和C%随温度的变化曲线如下图所示,下列说法正确的是
cC中物质的含量A%和C%随温度的变化曲线如下图所示,下列说法正确的是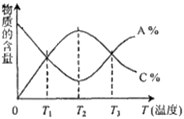
| A.该反应在T1、T3温度时达到化学平衡 |
| B.该反应在T1温度时达到化学平衡 |
| C.该反应为放热反应 |
| D.升高温度,平衡会向正反应方向移动 |