A、B、C、D、E是原子序数依次增大的5种短周期元素。A、E同主族,B、C是同周期相邻的两种元素。A、C的质子数之和等于D的质子数,A+离子与D2―离子的核外电子数之和等于E+ 离子的核外电子数。请回答下列问题:
(1)A、D元素按1 :1组成的化合物的结构式为_______ 。
(2)常见化合物W由A、D、E三种元素组成,则W中含有的化学键有_______ 。
若以W溶液为电解质溶液,铁棒为电极构成电解池,该电解反应的总反应方程式为: 。
(3)在恒容密闭容器中注入A2、C2两种气体,发生如下反应:3A2(g)+C2(g) 2CA3(g),在某温度下达到平衡时,各物质的浓度分别为:c(A2)=9.00mol/L;(C2)=3.00mol/L,c(CA3)=4.00mol/L。则C2的起始浓度为 mol/L;A2的转化率为_______ %0 。
2CA3(g),在某温度下达到平衡时,各物质的浓度分别为:c(A2)=9.00mol/L;(C2)=3.00mol/L,c(CA3)=4.00mol/L。则C2的起始浓度为 mol/L;A2的转化率为_______ %0 。
(4)A、C、D三种元素按原子个数比4︰2︰3形成的化合物溶于水,所得溶液呈酸性,用离子方程式解释其原因 。
(5)用E2D2在酸性条件下处理含CN―的工业废水,将得到N2及CO2等无污染的物质,请写出该反应的离子方程式_____________________ 。
磷是存在于自然界和生物体内的的重要元素。回答下列与磷及其化合物有关的问题。
(1)磷在自然界里主要以的形式存在于矿石中,这些磷矿石溶于水,其中的磷元素被作物吸收。
(2)磷(相对原子质量为31)在空气中燃烧生成的氧化物通常可用做强干燥剂。制备100g这种干燥剂所消耗的空气的体积约为L(在标准状况下)。
(3)有机磷农药“乐果”的结构简式是: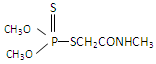 ,其中所含的双键有个。
,其中所含的双键有个。
1t下述氮肥的价格如下:尿素为1080元,硫酸铵为450元,硝酸铵为810元,碳酸氢铵为330元。分别用m元采购氮肥,购得的氮肥含氮元素最多的是。
自然界中的磷矿中,磷酸钙矿〔Ca3(PO4)2〕很少,主要是磷灰石矿〔Ca5F(PO4)3〕,写出由磷灰石矿粉为原料生产过磷酸钙肥料的反应方程式。
对十二烷基苯磺酸钠(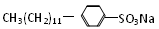 )是常用洗涤剂的主要成分。其结构可用图形“-”“○”来表示,左端为链烃基,右端为极性基。根据这一结构特点,试分析和回答下列问题。
)是常用洗涤剂的主要成分。其结构可用图形“-”“○”来表示,左端为链烃基,右端为极性基。根据这一结构特点,试分析和回答下列问题。
⑴该物质分子在其水溶液表面分布的结构示意图应是图1中的图(填写序号)。理由是。
⑵进入介质(水)内部的该物质的分子,可能会以图2所列的结构形式中的结构形式存在(填写序号)。理由是
如何除去下列物质中所含少量的杂质?写出所需试剂、分离方法及所用仪器。
| 混合物 |
所用试剂 |
分离方法 |
使用仪器 |
| ①肥皂水(甘油) |
|||
| ②乙酸乙酯(乙酸) |
|||
| ③硬脂酸(硬脂酸钠) |