(6分)金属镁有许多重要的用途,法国化学家维多克·格利雅因发明了在有机合成方面用途广泛的格利雅试剂而荣获诺贝尔化学奖,格利雅试剂的结构简式可表示为RMgX,它是金属镁和卤代烃反应的产物,简称格氏试剂,它在醚的稀溶液中以单体形式存在,并与二分子醚络合,在浓溶液中以二聚体存在,结构如下图: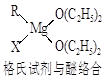
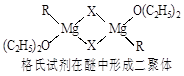
①标出格氏试剂 中的配位键
中的配位键
②下列比较中正确的是
A.金属键的强弱:Mg>Al B.基态原子第一电离能:Mg>Al C.金属性:Mg>Al
D.晶格能:KCl>NaCl E.电负性:Mg>Al F.硬度:Mg>Al
③二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。有关甲醛、苯、二氧化碳及水说法正确的是 。
A.苯与B3N3H6互为等电子体
B.甲醛、苯分子中碳原子均采用sp2杂化
C.苯、二氧化碳是非极性分子,水和甲醛是极性分子
D.水的沸点比甲醛高得多,是因为水分子间能形成氢键
金刚焼胺和达菲都是防治人传染禽流感的常有药。金刚烷胺结构式: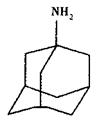
(1)金刚烷胺的分子式为_______。
(2)金刚烷胺的同分异构体中____(填“存在”或“不存在”)芳香族化合物。
生产达菲的主要原料是莽草酸,莽草酸存在以下转化关系: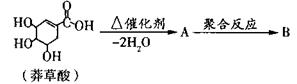
A含苯环,其苯环上若有一个氢原子被氯原子取代,将可能产生两种同分异构体。
(3)莽草酸→A的化学方程式:_______,该反应类型为_______。
(4)B的结构简式为_______。
(5)A的一种同分异构体水杨酸(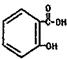 )也是医药工业的重要原料,下列有机物属于水杨酸同系物的是_______(填选项编号)。
)也是医药工业的重要原料,下列有机物属于水杨酸同系物的是_______(填选项编号)。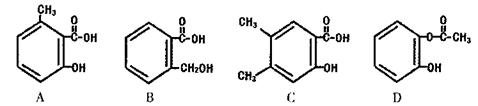
高锰酸钾是强氧化剂,它的用途遍布各个行业。
(1)工业上由软锰矿(主要成分为MnO2)生产髙锰酸钾分为两个步骤。
①步骤一将软锰矿与过量的固体KOH和空气在高温下反应,生成锰酸钾(K2MnO4),该反应的化学方程式是______________。
②步骤二以石墨为阳极,铁为阴极,电解锰酸钾(K2MnO4)溶液,在_______(填“阴极区”或“阳极区”)得到高锰酸钾。阴极反应的化学方程式是_______。
(2)某研究小组用工业生产高锰酸钾产生的废渣——猛泥(含K2MnO4、MnO2及Pb、Ca等元素)和乳钢废酸液制取工业级碳酸锰(MnCO3),其流程如下:
③轧钢废酸中Fe2+的作用是______________。
④操作I、操作II、操作III的名称是_______。
⑤溶液C中除含有Ca2+、Mn2+、H+外,还含有的阳离子是_______。
⑥若固体C中不含CaCO3,则溶液D中 <_______。
<_______。
[已知:Ksp(MnCO3)=1×10—11,Ksp(CaCO3)=5×10—9]
下表所列是元素周期表部分短周期的主族元素
| W |
X |
Y |
||
| R |
Z |
已知R为地壳中含量最多的金属元素。
(1)写出Z的原子结构示意图________。
(2)W与氢原子形成6原子分子的结构简式_______。
(3)超细RX粉末被应用于大规模集成电路领域。其制作原理为R2Y3、X2、W在高温下反应生成两种化合物,这两种化合物均由两种元素组成,且原子个数比均为1∶1;其反应的化学方程式为_______。
(4)X最高价氧化物对应水化物与X气态氢化物反应的生成物溶于水中,所得溶液离子浓度从大到小的顺序是_______。
(5)火箭发动机的燃料胼(N2H4)与氧化剂N2O4反应生成N2和水蒸气。
已知①N2(g)+2O2(g)=N2O4(l)△H1=—195kJ•mol—1
②N2H4(l) +O2(g)=N2(g)+2H2O(g)△H2=—534.2kJ•mol—1
写出肼和N2O4反应的热化学方程式______________。
(6)温度为T时,向2.0L恒容密闭容器中充入1.00 mol PCl5,反应PCl5(g)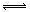 PCl3(g)+Cl2(g),经过一段时间(t)后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g),经过一段时间(t)后达到平衡。反应过程中测定的部分数据见下表:
| t/s |
0 |
50 |
150 |
250 |
350 |
| n(PCl3)/mol |
0 |
0.16 |
0.19 |
0.20 |
0.20 |
相同温度下,起始时向容器中充入1.00 mol PC15、0.20 mol PCl3和0.40 mol Cl2,反应达到平衡前v(正) _______v(逆)(填“>”或“=”或“<”);原因是_______。
莽草酸(C7H10O5)可有效对付致命的H5N1型禽流感病毒的药物“达菲”的重要成分,它可从中药八角茴香中提取得到。右图是以莽草酸为原料合成某些物质的路线: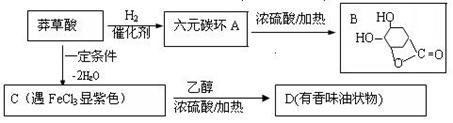
根据上图回答下列问题:
(1)A中含有的两种含氧官能团分别是_____________________
(2)已知烯醇式结构(C=C-OH)不能稳定存在、则莽草酸的结构简式为。
(3)莽草酸→C的反应类型是。
(4)写出C→D的化学反应方程式。
(5)与C具有相同官能团的同分异构体(含C)共有种。
(1)铬的外围电子排布式是,与铬同周期,最外层有3个未成对电子数的主族元素名称是,该元素对应的最低价氢化物分子的中心原子采取了杂化方式,分子的空间构型是 。
(2)富勒烯(C60)的结构如图,1molC60分子中σ键的数目为______ 。继C60后,科学家又合成了Si60、N60。请解释如下现象:熔点:Si60>N60>C60,而破坏分子所需要的能量: N60>C60>Si60,其原因是:。
(3)氟化氢水溶液中存在氢键有种。
(4)2011年诺贝尔化学奖授予了因发现准晶体材料的以色列科学家。某准晶体是锰与另一个短周期元素X形成的凝固态。已知:金属的电负性一般小于1.8。元素X与同周期相邻元素Y、Z的性质如下表:则X元素符号是,锰与X在准晶体中的结合力为。