合理膳食,保持营养均衡,合理使用药物是青少年学生健康成长的重要保证。
①维生素C能增强人体对疾病的抵抗能力,促进人体生长发育。在氯化铁溶液中加入维生素C溶液后,溶液由黄色转变为浅绿色,说明维生素C具有________性。
②________(填字母)具有止咳平喘作用,可用于治疗支气管哮喘、鼻粘膜充血引起的鼻塞等。
a.麻黄碱 b.阿司匹林 c.抗酸药 d.青霉素
③人们每天摄取的热能中大约有75%来自糖类,淀粉是一种重要的多糖,它在人体内水解的最终产物是________(填分子式)。碘元素是人体必需的微量元素之一,有“智力元素”之称,目前,我国通过在食盐中加入________(填化学式)从而达到补碘的效果。生物制药中往往涉及到活性蛋白质的提纯,可以采用的一种方法是________(填“过滤”、“高温蒸馏”或“盐析”)。淀粉、纤维素、油脂、蛋白质中不属于天然高分子的是________________。
为达到下表中的实验目的,请选择合适的试剂及实验方法,将其标号填入对应的空格。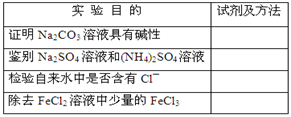
供选择的化学试剂及实验方法
| A.加入足量铁粉,过滤 |
| B.滴加酚酞试液,观察现象 |
| C.加稀HNO3和AgNO3溶液,观察现象 |
| D.加入NaOH浓溶液加热,观察现象 |
化学兴趣小组为探究某铁矿石(主要成分为Fe2O3和SiO2)的性质,进行如下实验: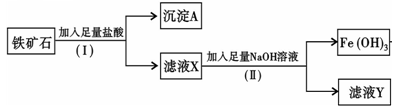
(1)步骤(I)中分离溶液和沉淀的操作名称是;
(2)沉淀A中一定含有,该物质属于(填“酸性”或“碱性”)氧化物;
(3)往滤液Y中加入KSCN溶液,溶液呈(填“黄色”或“红色”)
(4)写出步骤(Ⅱ)中生成Fe(OH)3的离子方程式。
完成下列各题
(1)工业上以氯气和石灰乳为原料制造漂白粉,漂白粉的有效成分是 __(填“CaCl2”或“Ca(ClO)2”)。
(2)某些合成染发剂含有对苯二胺(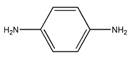 ),有一定的致癌作用。对苯二胺属于(填“有机物”或“无机物” )。
),有一定的致癌作用。对苯二胺属于(填“有机物”或“无机物” )。
取50.0mL K2CO3和K2SO4的混合溶液,加入过量BaCl2溶液后得到12.18g白色沉淀,用过量稀硝酸处理后沉淀量减少到2.33g,并有气体放出。试计算:
(1)原混合溶液中c(K2CO3) =;c(K2SO4) =;
(2)产生的气体在标准状况下的体积为。
实验室常用二氧化锰和浓盐酸反应制取氯气,反应式如下:
MnO2+ 4HCl(浓)=MnCl2+Cl2↑+2H2O
(1)用双线桥法表示上述反应中电子转移的方向和数目。
(2)反应中发生氧化反应的物质是___________(填化学式),被还原的元素是___________(填元素名称)。
(3)氧化剂与还原剂的物质的量之比为_________________。
(4)若反应中被氧化的盐酸为1mol,则生成的氯气体积为(标准状况下)。