为达到下表中的实验目的,请选择合适的试剂及实验方法,将其标号填入对应的空格。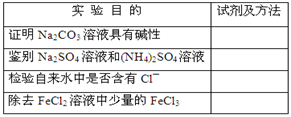
供选择的化学试剂及实验方法
| A.加入足量铁粉,过滤 |
| B.滴加酚酞试液,观察现象 |
| C.加稀HNO3和AgNO3溶液,观察现象 |
| D.加入NaOH浓溶液加热,观察现象 |
有以下几种物质①乙醇②MgCl2晶体③蔗糖④铜⑤食盐水⑥ BaSO4请填空回答(填序号)。
⑴以上物质中能导电的的是
⑵以上物质中属于电解质的是
⑶以上物质中属于非电解质的是
硫酸铵[(NH4)2SO4]是常见的氮肥,写出它在水中的电离方程式;施肥时,26.4g硫酸铵中能提供氮元素物质的量是,与克尿素[化学式CO(NH2)2]提供的氮元素质量相当。
若1.28克某气体XO2在标准状况下的体积为448mL,则X的摩尔质量为________,该气体可能是(填化学式)。
标准状况下,含有相同氧原子数的CO和CO2,其物质的量比为;质量比为;碳原子数比为;原子数比为;体积比为___________。
(8分)9.03×1023个H2O的质量是_____________g,其中含有____________molH,
含有___________g O,含有___________________个电子。