阿伏加德罗常数用NA表示,下列叙述正确的是
| A.18g D2O含有电子数为10 NA |
| B.NA个Fe(OH)3胶体粒子的质量为107 g |
| C.12g石墨中含有的σ键数目为3NA |
| D.常温常压下,S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2 NA |
某溶液中含有NH4+、Mg2+、Fe2+、A13+和SO42—五种离子,若向其中加入过量的Ba(OH)2溶液,微热并搅拌,再加入过量的氢碘酸,溶液中大量减少的离子有
| A.4种 | B.3种 | C.2种 | D.1种 |
若司机酒后驾车,可通过对其呼出的气体进行检验而查出,所利用的化学反应如下:2CrO3(红色)+3C2H5OH+3H2SO4=Cr2(SO4)3(绿色)+3CH3CHO+6H2O。关于该反应,下列叙述不正确的是
| A.每1 mol CrO3发生氧化反应,转移3 mol e— |
| B.C2H5OH是还原剂 |
| C.CrO3在反应中表现氧化性 |
| D.C2H5OH在反应中失去电子 |
下列化学用语正确的是
A.CH4分子的球棍模型: |
| B.乙烯的结构简式:CH2CH2 |
| C.氯化钠的分子式:NaCl |
D.K+的结构示意图: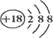 |
Fe和Fe2O3的混合物共13.6g,加入150mL稀H2SO4,在标准状况下收集到1.12LH2,Fe和Fe2O3均无剩余。为中和过量的H2SO4,并使Fe元素全部转化为Fe(OH)2沉淀,消耗了200mL 3mol/L的NaOH溶液,则该H2SO4的物质的量浓度为
| A.2.25mol/L | B.2mol/L | C.4mol/L | D.0.6mol/L |
下表各选项中,不能利用置换反应通过Y得到W的一组化合物是
| 选项化合物 |
A |
B |
C |
D |
| Y |
CO2 |
Fe2O3 |
SiO2 |
FeCl3 |
| W |
MgO |
Al2O3 |
CO |
CuCl2 |