依据元素周期表及元素周期律,下列推断正确的是
| A.同周期主族元素的原子形成的简单离子电子层结构相同 |
| B.C比Si的原子半径小,CH4的稳定性比SiH4弱 |
| C.Na、Mg、Al失电子能力和其最高价氧化物对应的水化物的碱性均依次减弱 |
| D.在元素周期表金属与非金属的分界处可以寻找催化剂和耐高温、耐腐蚀的合金材料 |
亚硝酸钠(NaNO2)可将人体血红蛋白中的Fe2+离子转化为Fe3+离子,生成高铁血红蛋白而丧失与氧气结合的能力,误食亚硝酸钠中毒,可服维生素C缓解。下列叙述中表现亚硝酸钠和维生素C的性质正确的是
| A.氧化性和还原性 | B.还原性和氧化性 |
| C.氧化性和酸性 | D.还原性和碱性 |
下列说法正确的是
| A.醋酸纤维、橡胶、腈纶都属于合成高分子化合物 |
| B.加新制的Cu(OH)2悬浊液并加热可检验尿液中的葡萄糖 |
| C.油脂在酸的催化作用下可发生水解,工业上利用该反应生产肥皂 |
| D.向蛋白质溶液中加入浓的Na2SO4或CuSO4溶液均可使蛋白质盐析而分离提纯 |
从海水中提取溴的反应原理是5NaBr + NaBrO3 + 3H2SO4 = 3Br2 + 3Na2SO4 + 3H2O,下列反应的原理与上述反应最相似的是
A 2NaBr + Cl2 =" 2NaCl" + Br2
B KClO3 + 6HCl 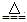 KCl + 3Cl2↑ + 3H2O
KCl + 3Cl2↑ + 3H2O
C 2H2S + SO2 =" 3S↓" + 2H2O
D AlCl3 + 3NaAlO2 + 6H2O = 4Al(OH)3↓ + 3NaCl
下列变化过程需要加入还原剂才能实现的是
A Na→NaOH B CO32-→CO2 C Fe2O3→FeD MnO4-→Mn2+
偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推动力。下列叙述正确的是
| A.偏二甲肼(C2H8N2)的摩尔质量为60g/mol |
| B.6.02×1023个偏二甲肼(C2H8N2)分子的质量与其摩尔质量相等 |
| C.1 mol 偏二甲肼(C2H8N2)中共含有12 mol原子 |
| D.6g偏二甲肼(C2H8N2)含有NA个偏二甲肼(C2H8N2)分子 |