向20 mL 0.5 mol·L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的相关说法中错误的是( )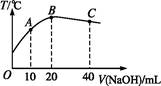
| A.醋酸的电离平衡常数:B点>A点 |
| B.由水电离出的c(OH-):B点>C点 |
| C.从A点到B点,混合溶液中可能存在:c(CH3COO-)=c(Na+) |
| D.从B点到C点,混合溶液中一直存在:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
下列热化学方程式中的反应热又为燃烧热的是 ( )
A.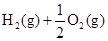 ══ ══ 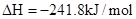 |
B.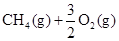 ══ ══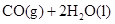 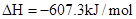 |
C.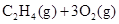 ══2CO2(g)+2H2O(l) ══2CO2(g)+2H2O(l)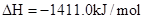 |
D.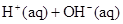 ══ ══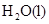 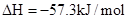 |
下列说法中正确的是()
| A.凡是放热反应都是自发的,吸热反应都是非自发的 |
| B.自发反应一定是熵增大,非自发反应一定是熵减小或不变 |
| C.熵增加且放热的反应一定是自发反应 |
| D.非自发反应在任何条件下都不能实现 |
醋酸溶液中存在电离平衡
 +
,不正确的是()
+
,不正确的是()
| A. | 醋酸溶液中离子浓度的关系满足:c( )=c( )+c( ) |
| B. | 常温下0.10 的 溶液中加水稀释,溶液中c( )减小 |
| C. | 溶液中加少量的 固体,平衡逆向移动 |
| D. | 常温下pH=2的 溶液与pH=12的 溶液等体积混合后,溶液的pH<7 |
下列说法不正确的是()
| A.比较多电子原子中电子能量大小的依据是电子离原子核的远近 |
| B.各能级最多容纳的电子数是该能级原子轨道数的二倍,其理论依据是构造原理 |
| C.电子排布在同一能级时,总是自由配对,优先占据同一轨道,且自旋方向相反 |
| D.钠的焰色与原子核外电子发生跃迁有关 |
具有相同电子层结构的三种微粒An+、Bn-和C,下列分析正确的是( )
A.原子序数关系:C>B>A
B.微粒半径关系:r(Bn-)<r(An+)
C.微粒C是稀有气体元素的原子
D.原子半径关系是:r(A)<r(B)<r(C)