有①Na2CO3溶液、②CH3COONa溶液、③NaOH溶液各25mL,物质的量浓度均为0.1mol/L,下列说法正确的是( )
| A.三种溶液pH的大小顺序是③>②>① |
| B.若将三种溶液稀释相同倍数,pH变化最大的是② |
| C.若分别加入25mL 0.1mol/L盐酸后,pH最大的是① |
| D.若三种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>② |
由乙醛和乙酸乙酯组成的混合物中,若含碳的质量分数为A%,则此混合物中含氢的质量分数为


























| A.6A% | B.10A % | C.(A/6)% | D.(100-7A/6)% |
有4种有机物:①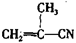 ②
②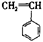 ③
③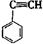 ④ CH3—CH=CH—CN,其中
④ CH3—CH=CH—CN,其中
 可用于合成结构简式为
可用于合成结构简式为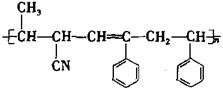 的高分子材料的正确组合为
的高分子材料的正确组合为
| A.①③④ | B.①②③ | C.①②④ | D.②③④ |
玻璃器皿上沾有一些用水洗不掉的残留物,其洗涤方法正确的是
①残留在试管内壁上的碘,用酒精洗涤②盛放过苯酚的试剂瓶中残留的苯酚,用酒精洗涤③做银镜反应后试管壁上银镜,用稀氨水洗涤④沾附在试管内壁上的油脂,用热碱液洗涤
| A.①③④ | B.②③④ | C.①②④ | D.①②③④ |
 下面四种变化中,有一种变化与其他三种变化类型不同的是:
下面四种变化中,有一种变化与其他三种变化类型不同的是:
A.CH3CH2OH + CH3COOH CH3COOCH2CH3 + H2O CH3COOCH2CH3 + H2O |
| B.CH2=CH2+H2O → CH3CH2OH |
C.2CH3CH2OH CH3CH2OCH2CH3 + H2O CH3CH2OCH2CH3 + H2O |
D.CH3CH2OH + HBr CH3CH2Br + H2O CH3CH2Br + H2O |
有关下图所示化合物的说法不正确的是


A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应 |
B.1 mol 该化合物最多可以与3 mol NaOH反应 |
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色 |
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体 |