已知相同条件下,HClO的电离常数小于H2CO3的第一级电离常数(Ka1)大于H2CO3的第二级电离常数(Ka2)。为了提高氯水中HClO的浓度,可行的是( )
| A.通入HCl(g) | B.加入NaHCO3(s) | C.加入H2O | D.加入NaOH(s) |
下列四个图像所反映的内容与相应反应符合的是(a、b、c、d均大于0)
密闭容器中进行的反应为 X(g)+3Y(g)  2Z(g),X、Y、Z 的起始浓度依次为0.1 mol/L,0.3 mol/L,0.2 mol / L,当反应达平衡时,各物质的浓度可能是
2Z(g),X、Y、Z 的起始浓度依次为0.1 mol/L,0.3 mol/L,0.2 mol / L,当反应达平衡时,各物质的浓度可能是
| A.X=0.2 mol / L | B.Y=0.5 mol  / L / L |
| C.Z=0.3 mol / L | D.Z=0.4 mol / L |
下列关于催化剂的说法,正确的是
| A.催化剂能改变化学反应进行的方向 | B.催化剂能改变化学反应进行的限度 |
C.催化剂能改 变化学反应的反应热 变化学反应的反应热 |
D.催化剂能改变化学反应的速率 |
反应A(g)+3B(g) 2C(
2C( g) ΔH<0,达到平衡后,将气体混合物的温度降低,下列叙述中正确的是
g) ΔH<0,达到平衡后,将气体混合物的温度降低,下列叙述中正确的是
| A.正反应速率和逆反应速率减小,平衡向逆反应方向移动 |
| B.正反应速率和逆反应速率减小,平衡向正反应方向移动 |
| C.正反应速率加大,逆反应速率减小,平衡向正反应方向移动 |
| D.正反应速率变小,逆反应速率增大,平衡向逆反应方向移动 |
已知反应aA(g)+bB(g)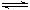 cC(g)+dD(g),右图表示在不同条件下生成物D的体积分数φ(D)随时间变化的关系,据此判断
cC(g)+dD(g),右图表示在不同条件下生成物D的体积分数φ(D)随时间变化的关系,据此判断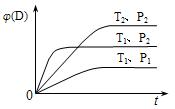
A.a+b<c+d,△H<0
B.a+b>c+d,△H>0
C.a+b<c+d,△H>0
D.a+b>c+d,△H<0