下列热化学方程式,正确的是:
| A.4g固体硫完全燃烧生成SO2,放出37 kJ热量:S(s)+O2(g)=SO2(g)ΔH= -296kJ/mol |
| B.1molN2与3molH2在某密闭容器中反应放出73kJ热量,则反应的热化学方程式为: N2(g)+3H2(g)  2NH3(g)△H= -73kJ/mol 2NH3(g)△H= -73kJ/mol |
| C.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g) ==CO2(g)+ 2H2O(g)ΔH=-890.3kJ·mol-1 |
| D.强酸强碱的中和热为- 57.3 kJ/mol: |
Ba(OH) 2(aq)+H2SO4(aq)=BaSO4(S)+2H2O(l) ΔH="-114.6" kJ/mol
下列离子方程式与所述事实相符且正确的是( )
| A.Ca(OH)2悬浊液中滴加足量稀硝酸:H++OH-=H2O |
| B.Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O |
| C.硫酸氢钠溶液中加入Ba(OH)2溶液至SO42-恰好完全沉淀:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
| D.向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应:4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2 |
同温同压下,质量忽略不计的两气球A和B,分别充入X气体和Y气体,且充气后两气球的体积相同.若相同条件下,A气球放在CO中静止不动,B气球放在O2中上浮.下列叙述或表示正确的是()
| A.X气体的相对分子质量比Y气体的相对分子质量大 |
| B.X可能是N2,Y可能是CH4 |
| C.X气体的密度小于Y气体的密度 |
| D.充气后A气球质量比B气球质量大 |
将0.1mol·L-1K2SO4溶液、0.2mol·L-1Fe2(SO4)3溶液与水混合,欲使混合溶液中K+、Fe3+、SO42-物质的量浓度为0.1mol·L-1、0.1mol·L-1、0.2mol·L-1,则所用的K2SO4溶液,Fe2(SO4)3溶液、水的体积比约为()
| A.1:1:1 | B.2:1:1 | C.1:1:2 | D.2:1:2 |
下列说法不正确的是( )
| A.5.85gNaCl晶体溶于100g水,所得溶液物质的量浓度不等于1mol/L |
| B.20g浓度为c mol·L-1的氨水中加入一定量的水稀释成0.5cmol·L-1,则加入水的体积小于20ml |
| C.某氯化镁溶液的密度为1.18 g·cm-3,其中镁离子的质量分数为5.1%,300 mL该溶液中Cl-的物质的量约等于1.50 mol |
D.V L Fe2(SO4)3溶液中含Fe3+m g,则溶液中SO42-的物质的量浓度为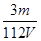 mol·L-1 mol·L-1 |
氧化还原反应实际上包含氧化和还原两个过程。(1)向氯酸钠的酸性水溶液中通入二氧化硫,该反应中氧化过程的反应式为:SO2+2H2O–2e-→SO42-+4H+;(2)向亚氯酸钠(NaClO2)固体中通入用空气稀释的氯气,该反应中还原过程的反应式为:Cl2+2e-→2Cl-。在(1)和(2)反应中均会生成产物X,则X的化学式为( )
| A.NaClO | B.NaClO4 | C.HClO | D.ClO2 |