下列有关海水综合利用的说法正确的是
| A.利用电解的方法可以从海水中获取淡水 |
| B.海水蒸发制海盐的过程只发生了化学变化 |
| C.从海水中可以得到NaCl,电解熔融NaCl可制备Cl2 |
| D.海水中含有钾元素,只需经过物理变化可以得到钾单质 |
木炭与浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是
| A.洗气瓶中产生的沉淀是碳酸钡 |
| B.Z导管出来的气体中无二氧化碳 |
| C.洗气瓶中产生的沉淀是硫酸钡 |
| D.Z导管口附近可能观察到红棕色出现 |
 下列各组物质中,化学键类型完全相同的是
下列各组物质中,化学键类型完全相同的是
| A.N2和NaOH | B.CO2和H2O | C.MgO和NaCl | D.HCl和KCl |
下列各组物质的性质依次递减的是
| A.碱性:Al(OH)3、Mg(OH)2、NaOH | B.还原性:HI、HBr、HCl |
| C.酸性:HClO4、H2SO4、H3PO4 | D.稳定性:H2CO3、NaHCO3、Na2CO3 |
可逆反应N2+3H2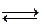 2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列各关系中能说明反应已达到平衡状态的是
2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列各关系中能说明反应已达到平衡状态的是
| A.3v正(N2)=v正(H2) | B.2v正(N2)=v逆(NH3) |
| C.v正(N2)=3v逆(H2) | D.2v正(H2)=3v逆(NH3) |
哈伯因发明用氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1molN2和3 molH2,在一定条件下使该反应发生。下列说法正确的是


A.达到化学平衡时,N2完全转化为NH3 |
B.一定条件下达到化学平衡后,反应体系中的压强保持不变 |
C.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化 |
D.达到化学平衡时,正反应和逆反应速率都为零 |