分某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了一系列实验,实验结果记录如下: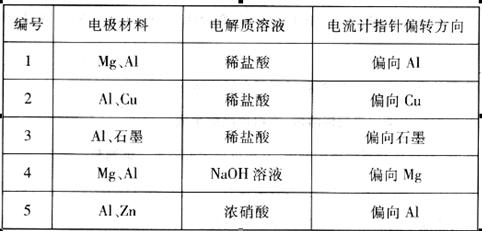
请根据上表中的实验记录回答下列问题:
(1)实验1、2中的Al所作的电极是否相同?____________________。
(2)在实验3中,Al作__________极,电极反应式为___________,电池总反应式为__________。
(3)实验4中的Al作正极还是负极?____________________,原因是____________________。
(4)解释实验5中电流计指针偏向Al的原因:__________________。
(5)根据实验结果,总结在原电池中金属铝作正极还是负极受到哪些因素的影响?____________________。

上图中
均为有机化合物,根据图中的信息,回答下列问题:
(1)环状化合物
的相对分子质量为82,其中含碳87.80%,含氢12.20%。
的一氯代物仅有一种,
的结构简式为;
(2)
是
的一种同分异构体,
能使溴的四氯化碳溶液褪色,分子中所有的碳原子共平面,则
的结构简式为;
(3)由
生成
的反应类型是,由
生成
的反应类型是;
(4)
的分子式为
,0.146g
需用
溶液完全中和,
是一种高分子化合物。则由
转化为
的化学方程式为;
(5)分子中含有两个碳碳双键,且两个双键之间有一个碳碳单键的烯烃与单烯烃可发生如下反应
则由
和
反应生成F的化学方程式为;
(6)
中含有的官能团是,
中含有的官能团是。

如图是一个用铂丝作电极,电解稀的
溶液的装置,电解液中加有中性红指示剂,此时溶液呈红色。(指示剂的
变色范围:6.8~8.0,酸色-红色,减色-黄色)
回答下列问题:
(1)下列关于电解过程中电极附近溶液颜色变化的叙述正确的是(填编号);
①
管溶液由红变黄;②
管溶液由红变黄;
③
管溶液不变色;④
管溶液不变色;
(2)写出
管中发生反应的反应式:;
(3)写出
管中发生反应的反应式:;
(4)检验
管中气体的方法是;
(5)检验
管中气体的方法是;
(6)电解一段时间后,切断电源,将电解液倒入烧杯内观察到的现象是。
、
、
、
、
、
、
、
、
是中学化学中常见的气体,它们均由短周期元素组成,具有如下性质:
①
、
、
、
、
能使湿润的蓝色石蕊试纸变红,
能使湿润的红色石蕊试纸变蓝,
、
、
不能使湿润的石蕊试纸变色;
②
和
相遇产生白色烟雾;
③
和
都能使品红溶液褪色;
④将红热的铜丝放入装有
的瓶中,瓶内充满棕黄色的烟;
⑤将点燃的镁条放入装有
的瓶中,镁条剧烈燃烧,生成白色粉末,瓶内壁附着黑色颗粒;
⑥
和
相遇生成红棕色气体;
⑦G在
中燃烧可以产生
和
;
⑧将
和
在瓶中混合后于亮处放置几分钟,瓶内壁出现油状液滴并产生
。
回答下列问题:
(1)
的化学式是,②中烟雾的化学式是;
(2)④中发生反应的化学方程式是 ;
;
(3)⑤中发生反应的化学方程式是;
(4)
的化学式是,
的化学式是;
(5)⑦中发生反应的化学方程式是;
(6)
的化学式是。
向2L密闭容器中通入a
气体
和b
气体B,在一定条件下发生反应;

已知:平均反应速率
;反应2
时,
的浓度减少了
,B的物质的量减少了
,有
生成。
回答下列问题:
(1)反应2
内,
=,
=;
(2)化学方程式中,
、
、
、
;
(3)反应平衡时,
为2a
,则
的转化率为;
(4)如果只升高反应温度,其他反应条件不变,平衡时D为1.5
,则该反应的
0;(填">"、"<"或"=")
(5)如果其他条件不变,将容器的容积变为1
,进行同样的实验,则与上述反应比较:
①反应速率(填"增大"、"减小"或"不变"),理由是;
②平衡时反应物的转化率(填"增大"、"减小"或"不变"),理由是;
(15分)有机化合物A~H的转换关系如下所示: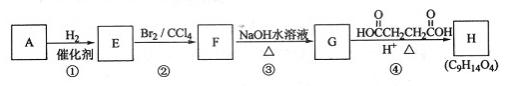
请回答下列问题:
(1)链烃A有南链且只有一个官能团,其相对分子质量在65~75之间,1 mol A完全燃烧消耗7 mol氧气,则A的结构简式是 ,名称是 ;
(2)在特定催化剂作用下,A与等物质的量的H2反应生成E。由E转化为F的化学方程式是 ;
(3)G与金属钠反应能放出气体,由G转化为H的化学方程式是 ;
(4)①的反应类型是 ;③的反应类型是 ;
(5)链烃B是A的同分异构体,分子中的所有碳原子共平面,其催化氢化产物为正戊为烷,写出B所有可能的结构简式
(6)C也是A的一种同分异构体,它的一氯代物只有一种(不考虑立体异构,则C的结构简式为 。