下列反应的离子方程式书写正确的是
| A.向Ba(OH)2溶液中滴入稀硫酸:H+ + OHˉ= H2O |
| B.向AlCl3溶液中滴入氨水:Al3++3OHˉ= Al(OH)3↓ |
C.向NaHCO3溶液中滴入稀盐酸:H++HCO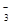 = CO2↑+H2O = CO2↑+H2O |
| D.向Fe2(SO4)3溶液中加入铁粉:Fe3++Fe = 2Fe2+ |
下列物质不属于高分子化合物的是()
| A.羊毛 | B.蚕丝 | C.橡胶 | D.蔗糖 |
右图是某分子的比例模型,黑色的是碳原子,白色的是氢原子,灰色的是氧原子。该分子是
| A.C2H5OH | B.C6H5OH | C.CH3CHO | D.CH3COOH |
下列有关实验操作、现象和解释或结论都正确的是( )
| 选项 |
实验操作 |
现象 |
解释或结论 |
| A |
过量的铁粉加入稀硝酸中,充分反应后,滴入KSCN溶液 |
溶液呈红色 |
稀硝酸将Fe氧化为Fe2+ |
| B |
AlCl3溶液中滴加过量的氨水溶液 |
先出现白色沉淀,后沉淀又逐渐溶解 |
氢氧化铝能溶于氨水 |
| C |
铝箔插入稀硝酸中 |
无明显现象 |
铝箔表面被稀硝酸氧化,形成致密的氧化膜 |
| D |
用玻璃棒蘸取浓硫酸点到pH试纸上 |
试纸变黑色 |
浓硫酸具有脱水性 |
工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2+ O2 2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是( )
2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是( )
| A.使用催化剂是为了加快反应速率,提高生产效率 |
| B.在上述条件下,SO2不可能100%地转化为SO3 |
| C.为了提高SO2的转化率,应适当提高O2的浓度 |
| D.达到平衡时,SO2的浓度与SO3的浓度相等 |
现有A、B、C、D四种金属片:
①把A、B用导线连接后同时浸入稀硫酸中,B表面变黑并逐渐溶解;
②把C、D用导线连接后同时浸入稀硫酸中,C发生氧化反应;
③把A、C用导线连接后同时浸入稀硫酸中,电子流动方向为A→导线→C。
根据上述情况,下列说法中正确的是( )
A.在①中,金属片B发生还原反应
B.在②中,金属片C作正极
C.如果把B、D用导线连接后同时浸入稀硫酸中,则金属片D上有气泡产生
D.上述四种金属的活动性由强到弱的顺序是:A>B>C>D