(8分) 某溶液由Na+、Cu2+、Fe3+、AlO2-、CO32-、SO42-、Cl-中的若干种离子组成。取适量该溶液进行如下实验:
①向其中加入过量的盐酸,有气体生成,并得到无色透明的溶液;
②在①所得的溶液中加入过量氨水,产生白色沉淀,过滤;
③在②所得的滤液中加入过量Ba(OH)2溶液,产生白色沉淀,过滤;
④在③所得的滤液中加入过量稀硝酸,再加入硝酸银溶液,产生白色沉淀。
根据以上实验回答下列问题:
(1)据①可知溶液中肯定存在的离子是 。
(2)③中反应的离子方程式为 。
(3)溶液中肯定不存在的离子是 。
(4)溶液中存在的溶质是 。
X、Y、Z、W是元素周期表前四周期中常见的元素,其相关信息如下表:
| 元素 |
相关信息 |
| X |
X的基态原子L层电子数是K层电子数的2倍 |
| Y |
Y的基态原子最外层电子排布式为:nsnnpn+2 |
| Z |
Z存在质量数为23,中子数为12的核素 |
| W |
W有多种化合价,其白色氢氧化合物在空气中会迅速变成灰绿色,最后变成红褐色 |
(1)W位于元素周期表第 周期第 族,其基态原子最外层有 个电子。
(2)X的电负性比Y的 (填“大”或“小”);X 和Y的气态氢化物中,较稳定的是 (写化学式)。
(3)写出Z2Y2与XY2反应的化学方程式,并标出电子转移的方向和数目:
(4)在X的原子和氢原子形成的多分子中,有些分子的核磁共振氢谱显示两种氢,写出其中一种分子的名称: 。氢元素,X、Y的原子也可共同形成多种分子和几种常见无机阴离子,写出其中一种分子与该无机阴离子反应的离子方程式: 。
有X、Y、Z、W四种化合物,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物、产物及反应条件已略去)。
(1)W的化学式是 ;
(2)X与Y在溶液中反应的离子方程式是: ;
(3)X Z过程反应的化学方程式是: 。
Z过程反应的化学方程式是: 。
(4)W经另一反应可转化为无色无味的单质气体Q,利用下图装置(夹持固定装置已略去)进行实验可在V中收集到Q,已知:烧瓶中固体为X或Z,装置III中产生白色沉淀。
则装置Ⅱ中物质的化学式___________,Ⅱ中主要反应的化学方程式是__________________。
某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图所示的变化。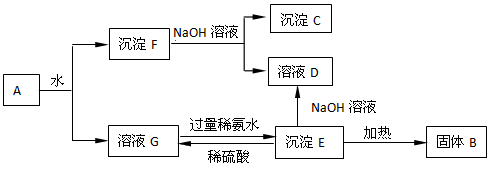
请回答下列问题。
(1)图中涉及分离溶液与沉淀的方法是_______________。
(2)写出以下4种物质的化学式为:B_________、C_________、D_________、E_________。
(3)沉淀F与NaOH溶液反应的离子方程式为__________________。
沉淀E与稀硫酸反应的离子方程式为__________________。
溶液G与过量稀氨水反应的化学方程式为_________________________。
如图中A到F是化合物,且A、B、E、F均含钠元素,G是单质.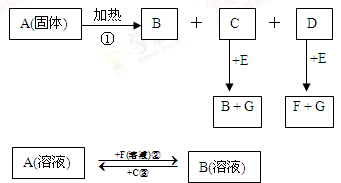
(1)写出A、B、E、F的化学式:A ________,B________,E________,F________.
(2)写出反应①②③的化学方程式:
①______________________________________;
②______________________________________;
③______________________________________。
A-I分别表示中学化学中的常见物质,它们之间的相互转化关系如下图所示(部分反应物、生成物没有列出),且已知G是一种两性氧化物,A、B、C、D、E、F六种物质中均含有同一种元素,F为红褐色沉淀。请填写下列空白: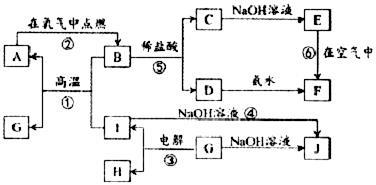
(1)A、B、C、D、E、F六种物质中所含的同一种元素是___________(写元素符号)。
(2)写出物质C、G的化学式:C___________,G___________。
(3)反应①的反应类型是: (填基本反应类型)。
(4)反应④的离子方程式: 。
(5)检验溶液D中金属阳离子的常用方法是: 。