(原创)科学家发现海洋是一个名副其实的“聚宝盆”,一些国家觊觎我国南海海域的丰富资源,导致近年来南海争端不断。下列对海洋资源开发利用的说法不正确的是
| A.海底如“土豆”般的金属结核矿含有铁、锰、钴等多种元素,可用铝热法冶炼并分离得到各种金属单质 |
| B.海水淡化工厂可与化工生产结合,如淡化后的浓海水,可用于提溴、镁、钠等 |
| C.海水中的金、铀等元素储量高、浓度低,提炼时,须先富集 |
| D.海水提镁过程中,所需的石灰乳,可用贝壳煅烧后加水得到,体现了就地取材、降低成本的生产理念 |
下列表述正确的是
| A.0.1mol·L-1Na2CO3溶液中:[OH-]=[HCO3-]+[H+]+[H2CO3] |
| B.0.1mol·L-1CH3COONa溶液中:[Na+]=[CH3COO-]+[OH-] |
| C.CH3COONa、NaOH和Na2CO3三种溶液的pH相同,则浓度大小顺序:c (NaOH) <c (Na2CO3) <c(CH3COONa) |
| D.向0.1mol·L-1CH3COOH溶液中滴加NaOH溶液至中性,溶液中离子浓度的关系:[CH3COO-]>[Na+]>[OH-]=[H+] |
下列离子方程式中,书写正确的是
A.弱酸酸式盐NaHB在水溶液中水解:HB–+H2O H3O++B2– H3O++B2– |
B.电解饱和食盐水:C1-+2H2O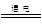 H2↑+Cl2↑+OH- H2↑+Cl2↑+OH- |
| C.氢氧燃料电池在碱性介质中的正极反应式:O2+2H2O+4e-=4OH- |
| D.FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
已知CH4(g)+2O2(g)→CO2(g)+2H2O(g) ΔH==- Q1 ;
2H2(g)+O2(g) →2H2O(g)ΔH==- Q2; H2O(g) →H2O(l)ΔH==- Q3
常温下,取体积比为4:1的甲烷和H2的混合气体112L(标准状况下),经完全燃烧后恢复到常温,则放出的热量为
| A.4Q1+0.5Q2 | B.4Q1+Q2+10Q3 | C.4Q1+2Q2 | D.4Q1+0.5Q2+9Q3 |
在四种化合物①NaHCO3②Al(OH)3③(NH4)2S④H2NCH2COOH中,跟盐酸和氢氧化钠溶液都能反应的是
| A.②④ | B.①② | C.①②③ | D.①②③④ |
对于锌一铜一稀硫酸组成的原电池装置中,当导线中有1 mol电子通过时,理论上的两极变化是
①锌片溶解了32.5g②锌片增重 32.5g③铜片上析出lg H2 ④铜片上析出1mol H2
| A.①和③ | B.①和④ | C.②和③ | D.②和④ |