(11 分)(原创)能源是人类生存和发展的重要支柱,研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义,已知下列热化学方程式
| |
① |
H2(g)+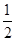 O2(g)= H2O(g) △H =﹣242kJ/mol; O2(g)= H2O(g) △H =﹣242kJ/mol; |
||||||||
| |
② |
2H2(g)+ O2(g)= 2H2O(l) △H =﹣572kJ/mol; |
||||||||
| |
③ |
C(s)+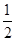 O2(g)= CO(g) △H =﹣110.5kJ/moL; O2(g)= CO(g) △H =﹣110.5kJ/moL; |
||||||||
| |
④ |
C(s)+ O2(g)= CO2(g) △H =﹣393.5kJ/moL; |
||||||||
| |
⑤ |
CO2(g)+ 2H2O(g)= CH4(g)+ 2O2(g)△H =" +" 802kJ/moL |
||||||||
| 化学键 |
O=O |
C-C |
H-H |
O-O |
C-O |
O-H |
C-H |
|
||
| 键能kJ/mol |
497 |
348 |
436 |
142 |
351 |
463 |
414 |
|
||
回答下列问题
(1)写出能表示H2燃烧热的热化学方程式 。
(2)已知C(s)+ H2O(g)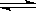 H2(g)+ CO(g)△H =" ___________" kJ/moL;
H2(g)+ CO(g)△H =" ___________" kJ/moL;
(3)估算出C=O键能为 kJ/moL。
(4)CH4的燃烧热△H = — ___________ kJ/moL。
(5)25℃、101kPa下,某燃具中CH4的燃烧效率是90%(注:相当于10%的CH4未燃烧),水壶的热量利用率是70%,则用此燃具和水壶,烧开1L水所需要的CH4的物质的量为_________mol[保留到小数点后2位;已知:c (H2O)=4.2J/(g·℃) ]。
(1)O22+与N2互为等电子体, O22+的电子式可表示为; O22+中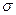 键数目和
键数目和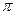 键数目之比为。
键数目之比为。
(2)将乙炔通入[Cu(NH3)2]Cl溶液生成红棕色沉淀Cu2C2。Cu+基态核外电子排布式为; Cu+的配位数为。
(3)乙炔与氢氰酸反应可得丙烯腈 。丙烯腈分子中碳原子轨道杂化类型是。
。丙烯腈分子中碳原子轨道杂化类型是。
(4)在合成氨反应中,催化剂铁表面上存在氮原子,如图为氮原子在铁的晶面上的单层附着局部示意图(图中小黑色球代表氮原子,灰色球代表铁原子)。则在图示状况下,铁颗粒表面上N/Fe原子数比为。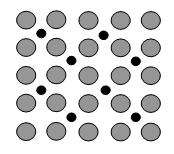
某化学反应 3 A(g)  2 B(g) + D(g),在四种不同条件下进行,B 、D的起始浓度为0。反应物A 的浓度 c 随时间 t 的变化情况如下表:
2 B(g) + D(g),在四种不同条件下进行,B 、D的起始浓度为0。反应物A 的浓度 c 随时间 t 的变化情况如下表: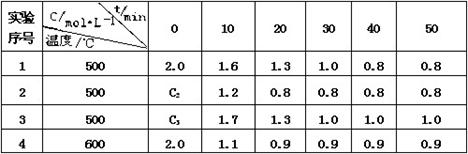
根据上述数据,完成下列填空:
(1)在实验 1,反应在10 min ~20 min 内平均速率v(A)为mol/(L·min)
(2)在实验 2 ,A 的初始浓度 C2 mol/L ,反应经 20 min 就达到平衡,可推测实验 2 中还隐含的条件是。
(3)设实验 3 的反应速率为v3,实验 1 的反应速率为v1,则v3 v1 (填<、>或=),
且C32.0 mol / L (填<、>或=)
(4)比较实验 4 和实验 1,可推测正反应是反应(填吸热或放热)。理由是
(5)该反应化学平衡常数表达式为。
a、b、c、d、e、f、g为七种由短期周期元素构成的粒子,它们都有10个电子,其结构特点如下:
| 粒子代码 |
a |
b |
c |
d |
e |
f |
g |
| 原子核数 |
单核 |
单核 |
双核 |
多核 |
单核 |
多核 |
多核 |
| 单位电荷数 |
0 |
1+ |
1- |
0 |
2+ |
1+ |
0 |
其中b的离子半径大于e的离子半径;d是由极性键构成的四原子极性分子;c与f可反应生成两个共价型g分子。试写出:
(1)d分子的空间构型为。
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为:>(用化学式表示)。
(3)d溶于水的电离方程式。
(4)g粒子所构成的晶体类型属。
(5)c粒子是,f粒子是(都用化学式表示)。
以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下: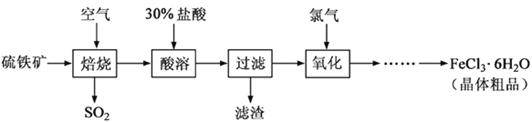
回答下列问题:
(1)硫铁矿高温焙烧的化学方程式为;少量的SO2与NaOH溶液反应的离子方程式为。
(2)酸溶及后续过程中均需保持盐酸过量,其目的是提高铁元素的浸出率和,
题问所涉及反应的离子方程式为。
(3)通氯气氧化时,发生的主要反应的离子方程式为;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为(写化学式)。
A是一种无色透明的晶体,进行如下实验:
①取少量A晶体做焰色反应实验,透过蓝色钴玻璃观察,火焰呈紫色。
②取少量A晶体溶于水可以得到无色的溶液,该溶液使石蕊变红。
③取少量A的溶液加过量氨水,有白色沉淀B生成。
④过滤除去③中的B后,在滤液中滴加氯化钡溶液,有白色沉淀C生成,C不溶于稀硝酸。
⑤取少量B滴加氢氧化钠溶液,得无色溶液D。
⑥取少量B滴加盐酸,得无色溶液E。
⑦将47.4 gA晶体在120 ℃下加热脱水,剩余物的质量为25.8 g。
根据上述实验现象和结果确定A、B、C、D、E,写出它们的化学式。
A:, B:, C:,
D:, E:。