(第1小题1分,其余每空2分,共11 分)
短周期元素A、B、C、D中,0.5 mol A元素的离子得到6.02×1023个电子被还原为中性原子,0.4 g A的氧化物恰好与100 mL 0.2 mol/L的盐酸完全反应,A原子核内质子数目与中子数目相等,B元素是第二周期中原子半径最小的元素,C2-比A元素的离子多1个电子层,D元素的原子核外L层比K层多2个电子。
(1)B元素的名称是 。
(2)画出D和C2-的结构示意图 。______________________。
(3)将B元素形成的单质通入水中反应的化学方程式为_________________________, B、C、D三种元素形成的氢化物中稳定性最强的是_______(填写化学式,下同),最高价氧化物的水化物酸性最强的是_______。
2,4,5-三氯苯酚和氯乙酸反应可制造除草剂2,4,5-三氯苯氧乙酸。某生产该除草剂的工厂曾在一次事故中泄漏出一种有毒的二恶英,简称TCDD。有关物质的结构式如下: 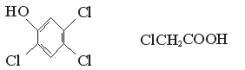
2,4,5-三氯苯酚氯乙酸 
2,4,5-三氯苯氧乙酸 TCDD
请写出:(1)生成2,4,5-三氯苯氧乙酸反应的化学方程式。
(2)由2,4,5-三氯苯酚生成TCDD反应的化学方程式。
氯普鲁卡因盐酸盐是一种局部麻醉剂,麻醉作用较快、较强,毒性较低,其合成路线如下: 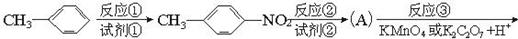
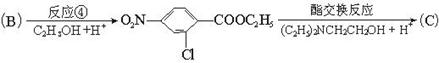
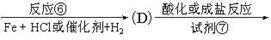

请把相应反应名称填入下表中,供选择的反应名称如下:
氯化、还原、硝化、磺化、氯代、酸化、碱化、成盐、酯化、酯交换、水解
| 反应编号 |
① |
② |
③ |
④ |
⑥ |
| 反应名称 |
(1)钠镁铝三种元素中第一电离能最大的是(填元素名称)。
(2)某正二价阳离子核外电子排布式为[Ar]3d54s0,该金属的元素符号为。
(3)微粒间存在非极性键、配位键、氢键及范德华力的是。
| A.NH4Cl晶体 |
| B.Na3AlF6晶体 |
| C.Na2CO3•10H2O晶体 |
| D.CSOu4溶液 |
E.CH3COOH溶液
(4)部分共价键键能数据如下表:
| 键 |
H-H |
N-H |
N-N |
N=N |
N≡N |
| 键能/kJ•mol-1 |
436 |
391 |
159 |
418 |
945 |
根据上表数据推算并写出氨气分解为氮气和氢气的热化学方程式:。
(5)乙醇和乙醚是同分异构体,但它们性质存在差异:
| 分子式 |
结构简式 |
熔点 |
沸点 |
水溶性 |
|
| 乙醇 |
C2H6O |
C2H5OH |
-114.3℃ |
78.4 °C |
互溶 |
| 二甲醚 |
C2H6O |
CH3OCH3 |
-138.5℃ |
-24.9℃ |
微溶 |
乙醇和二甲醚沸点及水溶性差异的主要原因是。
(6)金属铜溶于在浓氨水与双氧水的混合溶液,生成深蓝色溶液。该深蓝色的浓溶液中加入乙醇可见到深蓝色晶体析出,请画出呈深蓝色的离子的结构简式。
(7)石墨烯的应用为电子行业的发展带来了重大的突破,其结构可以看作是单层的石墨,其中碳原子的杂化方式为;C60的晶体结构类似于干冰,则每个C60晶胞的质量为(用含NA的式子表示)。
(14分)黄铁矿石的主要成分为FeS2和少量FeS(假设其他杂质中不含Fe、S元素,且高温下不发生化学变化),是我国大多数硫酸厂制取硫酸的主要原料。某化学兴趣小组对该黄铁矿石进行如下实验探究。将m 1 g该黄铁矿石的样品放入如下图装置(夹持和加热装置略)的石英管中,从a处不断地缓缓通入空气,高温灼烧黄铁矿样品至反应完全。其反应的化学方程式为:
4FeS2+11O2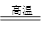 2Fe2O3+8SO24FeS+7O2
2Fe2O3+8SO24FeS+7O2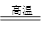 2Fe2O3+4SO2
2Fe2O3+4SO2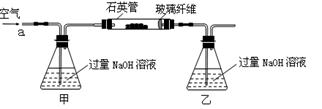
【实验一】:测定硫元素的含量反应结束后,将乙瓶中的溶液进行如下处理: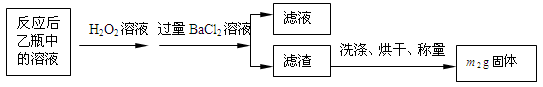
(1)鼓入空气的作用是__________________________________________。
(2)反应结束后乙瓶中的溶液需加足量H2O2溶液的目的是_______________(用化学方程式表示)。
H2O2可以看作是一种很弱的酸,写出其电离方程式:。
(3)该黄铁矿石中硫元素的质量分数为__________(列出表达式即可)。
【实验二】:测定铁元素的含量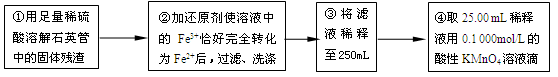
(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量_______(填“偏大”、“偏小”或“无影响”)。
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有_______。
(6)某同学一共进行了四次滴定实验,实验结果记录如下:
| 实验次数 |
第一次 |
第二次 |
第三次 |
第四次 |
| 消耗KMnO4溶液体积/mL |
25.00 |
25.03 |
20.00 |
24.97 |
根据所给数据,计算该稀释液中Fe2+的物质的量浓度为c(Fe2+) =___________。
I.碘钨灯具有使用寿命长、节能环保等优点。一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应: W(g)+ I2(g) WI2(g)
WI2(g)
为模拟上述反应,在实验室中准确称取0.508 g 碘、0.736 g金属钨放置于50.0mL密闭容器中,并加热使其反应。下图一是混合气体中的WI2蒸气的物质的量随时间变化关系的图像[n(WI2) ~ t]
其中曲线Ⅰ(0~t2时间段)的反应温度为450℃,曲线Ⅱ(从t2时刻开始)的反应温度为530℃。
请回答下列问题:
(1)该反应是(填写“放热”“吸热”)反应。
(2)反应从开始到t1(t1=" 3" min)时间内的平均速率υ(I2)=mol/(L.min)。
(3)在450℃时,计算该反应的平衡常数K=。
(4)能够说明上述反应已经达到平衡状态的有。
| A.I2与WI2的浓度相等 |
| B.单位时间内,金属钨消耗的物质的量与单质碘生成的物质的量相等 |
| C.容器内混合气体的密度不再增加 |
| D.容器内气体压强不变化 |
Ⅱ.图中甲为甲醇燃料电池(电解质溶液为KOH溶液),该同学想在乙中实现铁上镀铜,则a处电极上发生的电极反应式是。
Ⅲ.已知:H2(g)、CO(g)和CH3CH2OH(l)的燃烧热分别为285.8 kJ·mol-1、283.0 kJ·mol-1和1365.5 kJ·mol-1。反应 2CO(g)+4H2(g) CH3CH2OH(l)+H2O(l) 的△H=。
CH3CH2OH(l)+H2O(l) 的△H=。