向恒温、恒容(2L)的密闭容器中充入2molX和一定量的Y,发生反应:2X(g)+Y(g)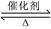 2Z(g)
2Z(g)
ΔH<0,4min后达到平衡c(X)=0.2mol·L-1,且X与Y的转化率相等。下列说法中不正确的是( )
| A.达到平衡时,再充入1molX,反应的焓变保持不变 |
| B.用Y表示4min内的反应速率为0.1 mol·L-1·min-1 |
| C.再向容器中充入1molZ,达到新平衡,c(X)∶c(Y)=2∶1 |
| D.4min后,若升高温度,平衡常数K增大 |
T℃时,在1 L的密闭容器中充入2 mol CO2和6 mol H2,一定条件下发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H="-49.0" kJ/mol
CH3OH(g)+H2O(g)△H="-49.0" kJ/mol
测得H2和CH3OH(g)的浓度随时间变化情况如下图所示。下列说法不正确的是
A.0~10 min内 (H2)="0.3" mol/(L·min) (H2)="0.3" mol/(L·min) |
| B.T℃时,平衡常数K=1/27,CO2与H2的转化率相等 |
| C.T℃时,反应中当有32 g CH3OH生成时,放出49.0 kJ的热量 |
| D.达到平衡后,升高温度或再充入CO2气体,都可以提高H2的转化率 |
下图是水煤气(成分为CO、H2)、空气燃料电池的工作原理示意图,a、b均为惰性电极。下列叙述中正确的是
| A.A处通入的是空气,B处通入的是水煤气 |
| B.a电极发生还原反应,b电极发生氧化反应 |
| C.如用这种电池电镀铜,待镀金属增重6.4 g,则至少消耗标准状况下的水煤气2.24 L |
| D.a电极的反应式包括:CO+4OH-+2e-=CO32-+2H2O |
室温下,下列图形与实验过程相符合的是
下列实验能达到预期目的的是
| A.从含I-的溶液中提取碘:加入硫酸酸化的H2O2溶液,再用酒精萃取 |
| B.检验溶液中是否一定含有CO32-:滴加稀盐酸,将产生的气体通入澄清石灰水 |
| C.检验蔗糖水解产物是否有还原性:向水解后的溶液中加入新制Cu(OH)2并加热 |
| D.除去粗盐溶液中的Ca2+、SO42-:依次加入过量的BaCl2溶液、Na2CO3溶液,过滤后再加适量盐酸 |
水热法制备纳米颗粒Y(化合物)的反应为
3Fe2++2S2O32-+O2+aOH-=Y+S4O62-+2H2O,下列说法中不正确的是
| A.a=4 |
| B.Y的化学式为Fe2O3 |
| C.S2O32-是还原剂 |
| D.每有1 mol O2参加反应,转移的电子总数为4 mol |